Наркоз, введение веществ крысам
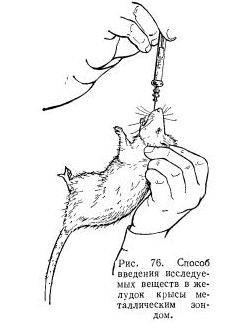
Наркоз. Для длительного обездвиживания наркотизированных крыс привязывают к операционному столику или к специальному станку. Ингаляционный наркоз у крыс с осторожностью можно проводить при помощи этилового эфира. Животное помещают под небольшой колпак, в камеру или эксикатор, куда кладут ватку, смоченную эфиром, и следят за наступлением наркоза. При помещении крыс (или мышей) в эксикатор или камеру для предотвращения удушья в них следует подавать воздух или кислород. При выполнении операций на сердце, легких, аорте крысы должны находиться на искусственном дыхании и у них проводят эндотрахеальный наркоз. Техника интубации трахеи у мелких лабораторных грызунов (хморских свинок, крыс и мышей), приспособления и устройства для ведения искусственного дыхания и эндотрахеального наркоза описаны А.X. Коганом (1978). Неингаляционный наркоз вызывают подкожным или внутрибрюшинным введением этаминала (внутрибрюшинно 40—50 мг/кг), барбамила (подкожно — 50—80 хмг/кг), хлоралгидрата (200—250 мг/кг) и других наркотиков. Способы введения исследуемых и лекарственных веществ. Оральное введение. Для введения в организм белой крысы порошкообразных веществ приготавливают пилюли, смешивая исследуемые вещества с мукой, хлебом или растворяя их в молоке. Пилюли дают подопытным крысам, рассаженным в отдельные клетки. Если животные отказываются поедать пилюли или молоко с примешанными препаратами, прибегают к принудительному введению при помощи зонда. Успокоенную крысу берут левой рукой за кожу в области затылка таким образом, чтобы большой палец находился у угла рта крысы. Левой ладонью слегка прижимают животное к столу и обездвиживают. Голову крысы кладут на левую сторону. Большой палец отодвигают кверху и назад, открывают при этом рот и начинают вводить резиновый зонд диаметром 2—3 мм, предварительно смоченный глицерином. Зонд должен идти над языком, по возможности ближе к щекам. Если продвижение зонда встречает препятствие, то его следует вынуть и вновь попытаться ввести. Вместо резинового зонда удобно пользоваться металлическим, изготовленным из иглы для шприца. Для этого острый конец иглы стачивают и на него напаивают головку из олова.
Полученный зонд следует слегка дугообразно изогнуть. Введение металлического зонда в желудок крысы не является затруднительным. Приученных к этой манипуляции крыс левой рукой удерживают за кожу в области затылка, придав им положение головой вверх. Большим и указательным пальцами натягивая щеки, открывают крысе рот. Металлический зонд, надетый на шприц и находящийся в правой руке, начинают вводить по задней стенке глотки, затем голову животного слегка опрокидывают кверху и назад (для этого указательным пальцем левой руки натягивают кожу головы в области затылка или между ушами), а зонд продвигают по ходу пищевода. Когда головка зонда находится в области шейного изгиба, то наружный конец его следует немного опустить (рис. 76). Обычно зонд проходит свободно и его введение не сопровождается осложнениями. Необходимо тщательно следить, чтобы головка зонда не имела острых выступов, Допустимо вводить до 1,5 мл жидкости.
Кожное введение. На коже, лишенной волосяного покрова, делают насечки скальпелем, скарификационной иглой или наждачной бумагой, после чего наносят исследуемый материал. Внутри кожное введение. В задней части спины или на животе выбривают шерсть или удаляют волосяной покров при помощи депилятория. Тоненькую иглу вводят в кожу на 1—3 мм, после чего инъецируют исследуемый раствор в количестве 0,02—0,04 мл. Подкожное введение. Помощник фиксирует животное. Шерсть на предполагаемом месте укола выстригают и дезинфицируют кожу. На спине или сбоку пальцами левой руки приподнимают кожу в виде складки, в основание которой затем делают укол. Иглу проводят параллельно складке. При введении больших количеств жидкости направление иглы нужно менять несколько раз. Взрослой крысе допустимо вводить под кожу до 10 мл жидкости. Внутримышечное введение чаше всего производят в мускулатуру бедра. Внутримышечно можно вводить до 5 мл жидкости. Прокол делают в освобожденный от волос и продезинфицированный участок кожи, чего нужно придерживаться и при внутрибрюшинном введении.
Внутрибрюшинное введение. Фиксированную крысу опускают вниз головой. Кожу живота каудальнее пупка берут в складку и у его основания прокалывают брюшную стенку, держа иглу перпендикулярно. В дальнейшем проводят иглу по ходу складки и производят инъекцию. Взятие брюшной стенки живота в складку и введение иглы по направлению складки предохраняют от повреждения иглой внутренние органы. Внутрибрюшинно можно вводить крысам до 5 мл жидкости. Внутривенное введение. Внутривенные инъекции производят в боковую вену хвоста тонкой иглой. Животное фиксируют одним из описанных способов. Для расширения вен хвост протирают ваткой, смоченной теплой водой, или опускают в теплую воду (45— 55 0C). Место укола высушивают и дезинфицируют. Хвост удерживают пальцами левой руки, а в правой держат шприц. Помощник сдавливает вену у корня хвоста. Прокол делают по возможности периферичнее, причем игла должна идти поверхностно по ходу вены. Если инъецированная жидкость не встречает сопротивления и в месте нахождения кончика иглы не отмечаются вздутия под кожей, то это указывает, что игла находится в сосуде (рис. 77).
Как и у морских свинок, внутривенное введение можно производить в дорсальную вену полового члена. Взрослым белым крысам внутривенно допустите вводить до 6 мл жидкости. Внутрисердечное введение. Пункция сердца описана ниже. Инъекцию следует проводить медленно. Внутрисердечно крысам допустимо вводить не более 1 мл жидкости. Субокципитальное введение производят наркотизированным животным. Техника проведения субокципитальной пункции такая же, как и у морских свинок и кроликов. Предварительно извлекают 0,1—0,2 мл спинномозговой жидкости. Допустимо вводить 0,05—9,15 мл жидкости. Для проведения инъекций у крыс используют иглы толщиной 0,45 мм.
Источник
Фиксация и введение морским свинкам исследуемых веществ (часть 3)
07.09.2012
Внутривенное введение растворов можно проводить в подкожную вену голени. Для этого находящееся под легким эфирным наркозом животное фиксируют спиной вверх, ножницами Купера срезают кожу по ходу вены выше скакательного сустава и отпрепаровывают ее от окружающей ткани. Вену сдавливают жгутом или помощник пережимает ее пальцами выше отпрепарированного участка. В вену вводят тоненькую иглу. Перед инъекцией насасыванием крови в шприц убеждаются, находится ли она в полости сосуда, после чего производят введение жидкости. Вводимый раствор при этом легко выдавливают из шприца. Если окружающие вену ткани начинают набухать, это свидетельствует о том, что игла вышла из сосуда или прошла сквозь его стенки.
Под наркозом внутривенные введения можно производить в бедренную или наружную яремную вены.
Иногда у отдельных животных при наличии хорошо выраженных вен уха можно в них вводить испытуемые растворы. Для этой цели пользуются очень тонкой иглой. Максимально допустимый объем жидкости при внутривенном введении морским свинкам составляет 4 мл.
Внутри сердечное введение. У морских свинок, находящихся в состоянии легкого наркотического сна, вызванного эфиром или барбитуратами, во втором межреберье слева, отступив на 2 мм от края грудины, производят пункцию сердца и, убедившись в том, что конец иглы находится в полости сердца, медленно производят инъекцию. Объем вводимой жидкости не должен превышать 1 мл.
Субокципитальное введение. Животное должно находиться под наркозом. Максимально сгибают голову. Производят пункцию в участке между затылочным бугром и остистым отростком атланта. При правильно проведенной пункции после извлечения мандрена из иглы вытекает спинномозговая жидкость. Извлекают 0,2—0,4 мл ликвора, после чего вводят неследуемый раствор. Допустимо вводить до 0,2 мл жидкости.
Внутри мозговое введение. Под эфирным наркозом у морской свинки производят трепанацию черепа. Место трепанации должно находиться на линии, соединяющей наружные углы глаз, несколько в сторону от срединной линии, чтобы не повредить фронтальный синус. Рекомендуется инъецировать жидкость не спеша, чтобы она не вытекала. Допустимо вводить до 0,2 мл раствора.
Для проведения инъекций морским свинкам рекомендуют пользоваться инъекционными иглами, имеющими толщину 0,5 мм.
Источник
Общая анестезия грызунов (практический опыт)
Растущая популярность содержания грызунов в последнее время вынуждает ветеринарных врачей осваивать необходимые технологии диагностики и лечения этих животных. Хирургические вмешательства и болезненные процедуры у грызунов часто требуют адекватного обезболивания.
Невозможно обеспечить достойный уровень ветеринарной помощи грызунам без качественной общей анестезии. В течение нескольких лет мы отрабатывали различные методики анестезии грызунов. Это было особенно сложно в свете действующих ограничений на использование наркотических и психотропных препаратов в ветеринарии. Конечно, очень удобно наркотизировать грызуна кетамином, но. увы.
На сегодняшний день нами отработана довольно эффективная и надежная схема анестезии крыс и морских свинок.
Мы применяем двухкомпонентный наркоз:
1. Внутримышечно или подкожно вводим ксилазин 20 мг/кг (0,1 мл/100 г веса животного). Через 10-15 минут можно переходить ко второму этапу.
2. Внутривенно вводим пропофол (диприван) 10 мг/кг (0,1 мл официнального раствора на 100 г живого веса). Вуаля!
В течение 15-30 минут после однократной инъекции пропофола можно спокойно проводить практически любые вмешательства, в т.ч. полостные, офтальмологические и ортопедические. При необходимости пропофол можно добавлять половинными дозами.
Отдельно о внутривенных инъекциях. Крыса и морская свинка — это, конечно, не доберман или ротвейлер: попадать грызунам в вену несколько сложнее, но вполне реально.
Мы пользуемся иглами — «бабочками» (scalp vein set) размер 26-27G. Пунктируем обычно подкожную вену внутренней поверхности бедра. Также доступна вена на краниальной поверхности предплечья. Многократно пытались пунктировать вены на ушах у морских свинок, — устойчивых результатов не получили. Определенные сложности возникают иногда с фиксацией животного во время внутривенной инъекции. Морские свинки, к счастью, кусаться не умеют, а крысы — напротив, могут причинить своими зубами существенный вред. Поэтому нелишне бывает завернуть переднюю часть туловища и голову крысы в плотную материю перед инъекцией.
Для удобства дозирования пропофол мы обычно разбавляем физиологическим раствором в 4-8 раз. Пропофол рекомендуем вводить медленно, наблюдая за реакцией животного. Иногда достаточно бывает1/2 — 2/3 расчетной дозы.
После инъекции иглу из вены не вынимаем и, по возможности, фиксируем для повторных инъекций.
Иногда на введение пропофола может развиться КРАТКОВРЕМЕННАЯ депрессия дыхания. В таких случаях можно несколько раз мануально форсировать движения грудной клетки. При использовании описанной схемы тяжелых анестезиологических осложнений мы не наблюдали ни разу.
Несколько слов о неудачном опыте анестезии. Внутрибрюшинная (вместо внутривенной) инъекция пропофола во многих случаях позволяет добиться необходимого уровня анестезии. Однако при таком введении очень сложно контролировать глубину и продолжительность наркоза. Вводить препарат необходимо в больших дозах (20-40 мг/кг). Также очень сильно различается время наступления анестезии (от 10 до 40 мин после инъекции). Депрессия дыхания, возникающая после внутрибрюшинной инъекции трудно поддается контролю — 2 животных у нас погибли.
Тем не менее внутрибрюшная анестезия пропофолом остается для нас основным методом при операциях у хомяков.
Будем рады узнать мнение коллег по данному вопросу, обсудить и обменяться мнениями в нашем форуме для специалистов.
Источник