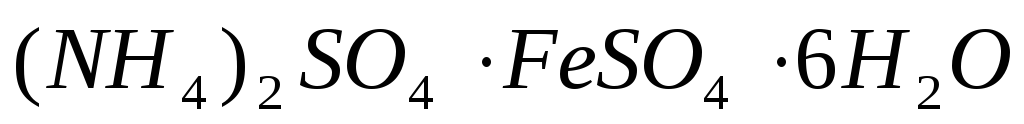1.3.3. Бихроматная окисляемость (ускоренный метод)
Определение бихроматной окисляемости может проводиться арбитражным и ускоренным методами. Оба метода являются титриметрическими. Ввиду сложности арбитражного метода определения ХПК ниже мы приводим только ускоренный метод, который можно считать упрощенной модификацией арбитражного. Приводимый метод вполне может быть реализован в полевых условиях или при отсутствии лабораторной базы (например, в производственных условиях) и пригоден для анализа сточных и загрязненных природных вод. Он нашел применение для постоянных ежедневных анализов, проводимых для контроля работы очистных сооружений, состояния воды в водоемах и др. Результаты определений, получаемые ускоренным методом, обычно несколько ниже, чем при анализах арбитражным методом, однако они хорошо воспроизводимы и коррелируют с его результатами. Воспроизводимость результатов, получаемых ускоренным методом, объясняется тем, что в одном и том же водоеме (сточной воде, технологической пробе и т.п.) присутствует практически один и тот же «букет» окисляемых органических соединений. Расхождения между результатами ускоренного и арбитражного методов могут быть значительными в тех случаях, когда в пробах присутствуют трудно окисляемые вещества – например, уксусная кислота, аланин, бензол и др. Практически же вводят коэффициент пересчета для корректировки результатов ускоренного метода и их приведения (с некоторой погрешностью) к арбитражному.
Главная особенность ускоренного метода определения ХПК – повышенная концентрация используемого раствора серной кислоты (применяется неразбавленная концентрированная серная кислота). В таких условиях не требуется специального нагревания пробы, т.к. ее температура повышается до необходимых значений за счет тепла, выделяемого при разбавлении серной кислоты. Именно в этом состоит основное отличие ускоренного метода от арбитражного, т.к. в последнем пробу необходимо кипятить более часа в сернокислотном растворе бихромата калия. Это создает ряд преимуществ ускоренного метода перед арбитражным, расширяет область его применения. Следует отметить, что при определении ХПК ускоренным методом окисление проводят без добавления катализатора – сульфата серебра. При этом несколько снижается точность анализа за счет неполного окисления части трудно окисляющихся органических веществ.
Ускоренный метод применяется при значениях ХПК не менее 50 мгО/л и не более 4000 мгО/л, при больших значениях пробу необходимо разбавить.
Оборудование и реактивы
Колба коническая плоскодонная из термостойкого стекла на 150-200 мл, пипетка-капельница, пипетки мерные, цилиндр мерный на 100 мл.
Вода дистиллированная или бидистиллированная, раствор бихромата калия (0,25 н.), раствор соли Мора титрованный, серная кислота концентрированная, сульфат ртути (II) кристаллический в капсулах по 0,2 г, раствор индикатора ферроина.
Примечание. Воду дистиллированную необходимо проверить на отсутствие органических веществ в холостой пробе.
О приготовлении растворов см. приложение 3.
Отбор и хранение проб
Количество пробы, отбираемой на анализ ускоренным методом, зависит от ожидаемого значения ХПК исследуемой воды. Соответствующие данные приведены в табл. 20.
Количество пробы для анализа
Источник
Лабораторная работа №2 Определение миллиграммового содержания железа (II) в солях, рудах и технических материалах
Ионы железа (II) легко окисляются перманганатом калия в кислой среде до иона железа (III) по реакции:
MnO4 — + Fe 2+ + 8H + = Mn 2+ + 5Fe 3+ + 4H2O
Если для анализа дан твердый образец, то его предварительно надо измельчить и растворить в соответствующем растворителе (чаще всего в кислоте). Если исследуемый раствор содержит примеси железа (III) и если нужно определить железо (III) перманганатометрически, то его предварительно необходимо восстановить до железа Fe 2+ , для чего используют хлорид олова (II) в солянокислой среде.
- Заполнить бюретку раствором KMnO4 известной нормальности и установить уровень жидкости на нуле по верхнему мениску.
- В мерную колбу на 100 мл получить неизвестный объем раствора соли железа (II), довести до метки дистилированной водой и тщательно перемешать.
- В две колбы для титрования на 200-250 мл прилить пипеткой на 15 или 20 мл аликвоту анализируемого раствора из мерной колбы.
- В эти же колбы прилить цилиндром по 15 мл 2н H2SO4.
- Титровать содержимое колбы раствором перманганата при комнатной температуре до появления неисчезающей в течение 30 с бледно-розовой окраски. Раствор титранта KMnO4 приливать с такой скоростью, чтобы капли можно было сосчитать.
- Записать объемы по бюретке (V1 и V2) соответственно титрованию первой и второй колб и рассчитать средний арифметический объем:
(V1+V2)/2 =Vср.
- Вычислить с точностью до четырех значащих цифр массу железа (II) в миллиграммах по формуле:
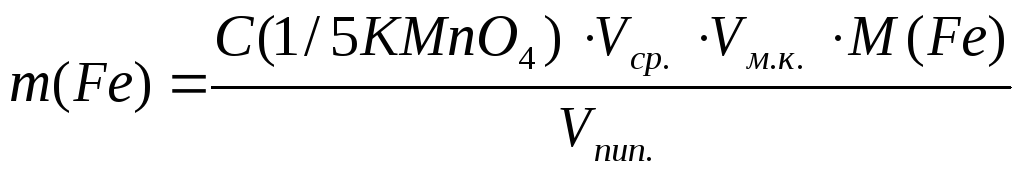
- Показать преподавателю выполненную работу, получить у него правильный результат и вычислить процент относительной ошибки:
% отн. ошибки = 
Лабораторная работа №3 Определение миллиграммового содержания хрома в бихромате калия методом обратного титрования
Бихромат калия (K2Cr2O7) не вступает в прямое взаимодействие с перманганатом калия, так как сам является сильным окислителем (φ 0 = 1,36 В). Поэтому для определения хрома в бихромате методом перманганатометрии прибегают к обратному титрованию. В качестве промежуточного вещества-восстановителя используется раствор соли Мора, где железо имеет окислительное число, равное двум.
План работы
- В мерную колбу на 100,00 мл получить контрольный объем бихромата калия, довести до метки дистилированной водой, перемешать.
- В две колбы для титрования на 250 мл прилить пипеткой на 15 или 20 мл аликвоту из мерной колбы.
- В эти же колбы прилить цилиндром по 20 мл 2н раствора серной кислоты.
- Из бюретки на 50,00 мл прилить в каждую колбу по 30,00 мл соли Мора (заведомый избыток). Оставить смесь на 5 минут для завершения реакции.
K2Cr2O7 + 6FeSO4 + 7H2SO4 = Cr2(SO4)3 + 3Fe2(SO4)3 + K2SO4 + 7H2O(7)
| 1 | Cr2O7 2- + 14H + + 6e = 2Cr 3+ + 7H2O |
| 3 | 2Fe 2+ — 2e = 2Fe 3+ |
- Заполнить бюретку титрованным раствором перманганата калия и довести уровень жидкости до нуля по верхнему мениску.
- По истечении 5 минут разбавить содержимое колбы дистилированной водой приблизительно вдвое для ослабления зеленой окраски соли сульфата хрома (III).
- Титровать остаток соли Мора, не вошедший в реакцию с бихроматом калия, раствором перманганата до почти бесцветной (серой) окраски (такая окраска получается в результате наложения зеленого и розового цветов).
- Записать объемы KMnO4по бюреткеV1иV2, пошедшие на титрование остатка соли Мора в колбах 1 и 2 и вычислить среднеарифметический объем:
(V1+V2)/2 =Vср.(KMnSO4)
- Железо (II) в растворе соли Мора при хранении окисляется кислородом воздуха, поэтому точную нормальность этого раствора обычно не устанавливают, а проводят контрольное титрование. Цель такого титрования – определить объем перманаганатаVконтр., необходимый для титрования всего объема соли Мора (30 мл).
- Контрольное титрование. В две колбы для тирования прилить из большой бюретки на 50,00 мл по 15,00 мл соли Мора, сюда же цилиндром прилить по 15 мл 2н раствора серной кислоты и титровать перманганатом до слаборозового цвета, записать полученные объемы V1иV2, вычислить среднее значение объемаVср.и умножить его на два: 2Vср.=Vконтр(KMnSO4).
- Объем KMnO4, пошедший на реакцию с аликвотой бихромата калия, найти по разнице (Vконтр. -Vср.).
- Вычислить с точностью до четырех значащих цифр содержание хрома в бихромате калия в миллиграммах:
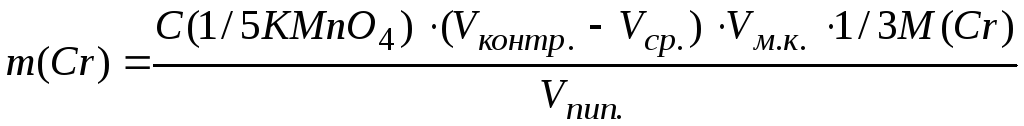
Источник