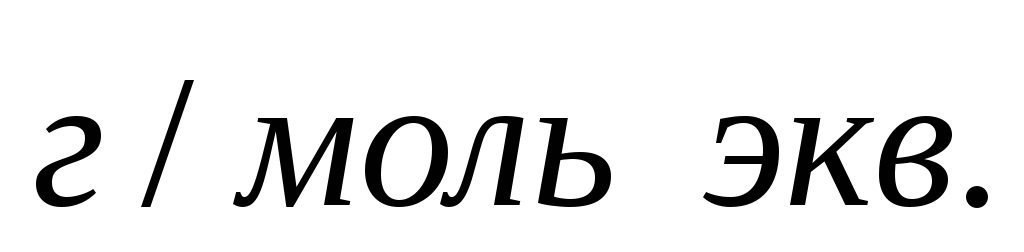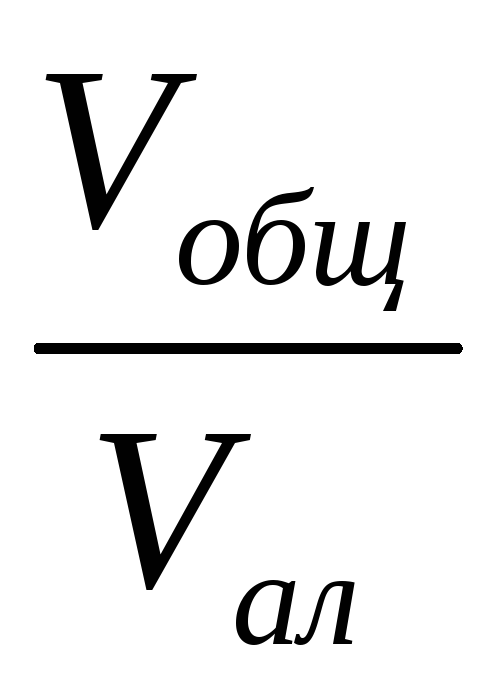- Лабораторная работа 9 Стандартизация рабочего раствора перманганата калия. Определение содержания железа в соли Мора
- Методика определения концентрации (стандартизация) раствора соли Мора.
- Лабораторная работа №13
- Приготовление стандартного раствора бихромата калия
- Приготовление контрольного раствора соли Мора
Лабораторная работа 9 Стандартизация рабочего раствора перманганата калия. Определение содержания железа в соли Мора
Методы редоксиметрии основаны на применении реакций окисления-восстановления. Рабочими растворами в оксидиметрии являются растворы окислителей или восстановителей. Следовательно, этими методами можно проводить количественные определения восстановителей и окислителей.
Необходимым условием протекания окислительно-восстановительной реакции является наличие разности потенциалов (редокс-потенциалов) у реагирующих пар (пара — окисленная и восстановленная форма окислителя или восстановителя). Зная величины стандартных редокс-потенциалов (Е о ) реагирующих пар, можно судить о направлении окислительно-восстановительных реакций. Окисленная форма пары с большим стандартным редокс-потенциалом является окислителем по отношению к восстановленной форме пары с меньшим потенциалом.
Редокс-потенциал какой-либо пары зависит от концентраций окисленной и восстановленной форм, реакции среды, температуры и т.д. Его можно рассчитать по уравнению Нернста:
E = E o + 0,06/n∙lg[Oк.]/[Восст.],
где [Oк.] – концентрация окисленной формы; [Восст.] – концентрация восстановленной формы; n – количество электронов, участвующих в полуреакции.
Реакция используется в количественном анализе, если разность потенциалов реагирующих пар (ЭДС системы) имеет значение 0,4-0,5 В.
Методы редоксиметрии, в зависимости от используемых титрантов, подразделяются на:
1. Перманганатометрия. Титрант — раствор перманганата калия KMnO4. Индикатор — избыточная капля титранта.
2. Иодометрия. Титрант — раствор свободного иода I2 или тиосульфата натрия Na2S2O3. Индикатор — крахмал.
3. Дихроматометрия. Титрант — раствор дихромата калия K2Cr2O7 и другие методы.
Вычисления молярных масс эквивалентов окислителей и восстановителей проводят по формуле: Мэ = М/n, где n ˗ число электронов, которые присоединяет или отдает в данной реакции один моль вещества. То есть, для нахождения молярной массы эквивалента окислителя (восстановителя) нужно его молярную массу разделить на число принятых (отданных) электронов в данной полуреакции.
Например, в реакции окисления сульфата железа (II) перманганатом калия в кислой среде:
1 MnO4 — + 8 H + + 5 e Mn 2+ + 4 H2O
ион MnO4 — как окислитель принимает пять электронов, а ион Fe 2+ как восстановитель отдает один электрон. Поэтому для расчета молярных масс эквивалентов окислителя и восстановителя их молярные массы следует разделить на пять и на один, соответственно.
Mэ(KMnO4) =
Мэ(FeSO4) = Mэ(Fe 2+ ) = M(Fe 2+ ) = 55,85 г/моль
В реакции окисления сульфита натрия перманганатом калия в нейтральной среде:
ион MnO4 — принимает только три электрона, а ион восстановителя SO3 2- отдает два электрона, следовательно:
Mэ(KMnO4) = 
Из приведенных примеров видно, что молярные массы эквивалентов окислителей и восстановителей зависят от условий проведения реакций и определяются, исходя из соответствующих полуреакций. Рома! Это можно убрать или переставить в лаб раб ОВР
Метод основан на окислительно-восстановительных реакциях, в которых окислителем является перманганат-ион MnO4 — .
Перманганат калия проявляет окислительные свойства в кислой, нейтральной и щелочной средах:
MnO4 — + 8H + + 5e Mn 2+ + 4H2O Е о = 1,51 В
MnO4 — + 2H2O + 3 e MnO2 + 4OH — Е о = 0,59 В
MnO4 — + 1 e MnO4 2- Е о = 0,56 В
Титрование перманганатом калия проводят в кислых средах, поскольку окислительная активность перманганата калия в кислой среде гораздо выше, чем в нейтральной и щелочной. При восстановлении перманганат-ионы в кислой среде превращаются в ионы Mn 2+ и раствор обесцвечивается. Это позволяет легко фиксировать точку эквивалентности за счет розовой окраски избыточной капли самого перманганата калия.
Восстановители обычно определяются методом прямого титрования их раствором перманганата калия. Окислители ˗ методом обратного титрования. В этом случае раствором перманганата калия оттитровывают избыток восстановителя, приливаемого к окислителю.
Индикатором в этом методе служит сам рабочий раствор ˗ перманганат калия.
Экспериментальная часть
Стандартизация рабочего раствора перманганата калия
Перманганат калия обычно содержит ряд примесей, поэтому раствор, приготовленный по навеске, не имеет точной концентрации.
Раствор перманганата калия должен храниться в склянке из темного стекла, так как под действием света происходит его разложение:
Поэтому через 5-7 дней после приготовления раствор перманганата калия отфильтровывают через стеклянный фильтр и проводят его стандартизацию.
Молярную концентрацию эквивалентов раствора перманганата калия обычно устанавливают по стандартному раствору перекристаллизованной щавелевой кислоты Н2С2О4 . 2Н2О.
Стандартизация раствора перманганата калия по щавелевой кислоте
Реакция между перманганатом калия и щавелевой кислотой в сернокислой среде протекает по следующему уравнению:
2 MnO4 — + 8 H + + 5 e Mn 2+ + 4 H2O
Порядок выполнения работы
1. Ополоснуть и наполнить бюретку раствором перманганата калия. Установить уровень жидкости на нулевом делении по верхнему краю мениска (для окрашенных жидкостей уровень устанавливается по верхнему краю мениска). Заполнить кончик бюретки.
2. В колбу для титрования цилиндром налить 15 мл 1 М раствора серной кислоты H2SO4 и 25 мл дистиллированной воды. Колбу на 2-3 минуты поставить на водяную баню нагретую до 70-80 о С. Чистую пипетку ополоснуть раствором щавелевой кислоты. Отмерить пипеткой точный объем раствора щавелевой кислоты H2C2O4 и перенести его в колбу для титрования c нагретым раствором серной кислоты.
3. Оттитровать горячий раствор щавелевой кислоты перманганатом калия. Катализатором реакции служат ионы Mn 2+ , которые являются одним из продуктов реакции. В начале титрования реакция идет медленно, первые капли перманганата обесцвечиваются с трудом. Поэтому прибавление первого миллилитра перманганата нужно проводить очень медленно. После того как образовались ионы Mn 2+ , скорость реакции увеличивается, и титрование можно вести быстрее, прибавляя перманганат калия маленькими порциями и сильно перемешивая раствор в колбе. Новая порция прибавляется только после обесцвечивания предыдущей. Конец титрования определяется по появлению неисчезающей в течение 1-2 минут бледно-розовой окраски от одной лишней капли перманганата калия. Взятый объем щавелевой кислоты и объем перманганата калия, пошедший на титрование, записать в таблицу.
4. Результаты титрования записать в таблицу. Повторить титрование до получения сходящихся результатов.
5. Рассчитать молярную концентрацию эквивалента и титр раствора перманганата калия.
Форма лабораторного отчета
Лабораторная работа № . Дата
“Название лабораторной работы”
Определяемое вещество (титрант) — СЭ(KMnO4) = ?, T(KMnO4) = ?
Индикатор – избыточная капля раствора KMnO4
Условия титрования — (рН среды, нагревание и т.д.)
Уравнение реакции (в молекулярной и ионно-молекулярной формах):
Источник
Методика определения концентрации (стандартизация) раствора соли Мора.
Бюретку ополоснуть раствором KMnO4, затем заполнить ее раствором KMnO4 до 0 (носик бюретки должен быть заполнен раствором KMnO4). Другую бюретку ополоснуть раствором соли Мора, затем заполнить ее раствор соли Мора до 0 (носик бюретки должен быть заполнен раствором соли Мора). Коническую колбу ополоснуть дистиллированной водой. С помощью бюретки отобрать аликвоту стандартного раствора (10,00мл) соли Мора, перенести в коническую колбу, прилить 3-5мл H3PO4 и оттитровать раствором KMnO4 до появления слабо розовой окраски в точки эквивалентности. Титрование повторяить не менее 3-х раз. Вычислить средний объём KMnO4, пошедший на титрование соли Мора. По результатам титрования рассчитать точную концентрацию стандартного раствора соли Мора.
6.1. Пример вычисления точной концентрации стандартного раствора соли Мора Сн(NH4)2Fe(SO4)2·6H2O по «Глухому опыту»
На титрование 10,00мл раствора соли Мора пошло 9,70мл раствора KMnO4 (средний объём). Вычислить Сн (NH4)2Fe(SO4)2·6H2O, если Сн(KMnO4) = 0,05103моль/л.
| Дано: Сн (KMnO4) = 0,05103 моль/л V(KMnO4) = 9,70 мл V (NH4)2Fe(SO4)2·6H2O = 10,00 мл Мэ (NH4)2Fe(SO4)2· 6H2O = =М=392,13 г/моль |
| mн-? |
7. Методика определения массовой доли K2Cr2O7 в техническом образце дихромата калия.
Коническую колбу ополоснуть дистиллированной водой. Пипетку ополоснуть раствором дихромата калия. Пипеткой отобрать аликвоту раствора (10,00мл) дихромата калия, перенести в коническую колбу, прилить из бюретки 20,00мл стандартного раствора соли Мора, 3-5мл раствора H3PO4. Реакционную смесь в конической колбе перемешать и через 2-3 минуты остаток стандартного раствора соли Мора (не вступившего в реакцию) оттитровать стандартным раствором метода перманганатометрии — раствором KMnO4 до появления бледно розовой окраски на серо-зелёном фоне в точке эквивалентности. Провести титрование не менее 3-х аликвот анализируемого раствора K2Cr2O7. Вычислить средний объём KMnO4, пошедший на титрование остатка соли Мора.
8. Вычисление массовой доли дихромата калия K2Cr2O7 в техническом образце
Навеску технического дихромата калия массой 0,3010г количественно перенесли и растворили в мерной колбе ёмкостью 100мл. 10,00 мл полученного раствора обрабатывают 20,00мл стандартного раствора соли Мора. На титрование остатка соли Мора, не вступившего в реакцию, ушло 8,60мл раствора KMnO4 (средний объём) с Сн (KMnO4) = 0,05103моль/л. Вычислите массовую долю K2Cr2O7 в техническом образце, если Сн(NH4)2Fe(SO4)2·6H2O, вычисленная на основании «глухого опыта» составила 0,04950 моль/л
| Дано: Сн (KMnO4) = 0,05103 моль/л Сн (NH4)2Fe(SO4)2*6H2O = 0,04950 моль/л mн= 0,3010 г Vк = 100 мл V (K2Cr2O7) = 10,00 мл V (NH4)2Fe(SO4)2*6H2O = 20,00 мл V (KMnO4) = 8,60 мл Мэ (K2Cr2O7) = М/6 = 49,03 г/моль | 1 способ по контрольному опыту («глухому опыту») Из глухого опыта 10,00 мл соли Мора эквивалентны 9,70 мл KMnO4 1) 1)Сколько мл KMnO4 эквивалентно 20,00 мл соли Мора? 10,00 мл соли Мора эквивалентно 9,70 мл KMnO4 20,00 мл соли Мора эквивалентно Х мл KMnO4 2) 2)Сколько мл KMnO4 эквивалентно K2Cr2O7? 19,40 — 8,60 = 10,80 мл 3) 1) Сколько моль-экв KMnO4 содержится в 1 мл раствора? 2) Сколько моль-экв KMnO4 содержится в 10,80 мл раствора? Столько же моль-экв K2Cr2O7 содержится в 10,00 мл раствора. 3) Сколько моль-экв K2Cr2O7 содержится в 1 мл раствора? 4) Сколько моль-экв K2Cr2O7 содержится в 100 мл раствора? 5) Сколько г K2Cr2O7 содержится в 100 мл раствора? Столько же г K2Cr2O7 содержится в навеске. 6) Сколько г K2Cr2O7 содержится в 1 г образца? 7) Сколько г K2Cr2O7 содержится в 100 г образца или w (K2Cr2O7)? 2 способ – по количеству моль-экв |
| w (K2Cr2O7) -? | |
| 1) Сколько моль-экв соли Мора содержится в 20,00 мо раствора? 2) Сколько моль-экв KMnO4 содержится в 8,60 мо раствора? Столько же моль-экв соли Мора содержится в остатке. 3) Сколько моль-экв соли Мора пошло на взаимодействие с K2Cr2O7? Столько же моль-экв K2Cr2O7 содержится в 10,00 мл раствора. 4) Сколько моль-экв K2Cr2O7 содержится в 1 мл раствора? 5) Сколько моль-экв K2Cr2O7 содержится в 100 мл раствора? 6) Сколько г K2Cr2O7 содержится в 100 мл раствора? Столько же г K2Cr2O7 содержится в навеске. 7) Сколько г K2Cr2O7 содержится в 1 г образца? 8) Сколько г K2Cr2O7 содержится в 100 г образца или w (K2Cr2O7). |