БРОМ
БРОМ (от греч. bromos — зловоние; название связано с неприятным запахом брома; лат. Bromum) Br, хим. элемент VII гр. периодич. системы, ат. н. 35, ат. м. 79,904; относится к галогенам. Прир. бром состоит из стабильных изотопов 79 Вr (50,56%) и 81 Вr (49,44%). Конфигурация внеш. электронной оболочки 4s 2 4p 5 ; степени окисления — 1 (бромиды), + 1 (гипобромиты), + 3 (бромиты), + 5 (броматы) и + 7 (перброматы); энергия ионизации при последоват. переходе от Вг° до Вг 7+ соотв. 11,84, 21,80, 35,90, 47,3, 59,7, 88,6, 109,0, 192,8 эВ; электроотрицательность по Полингу 2,8; атомный радиус 0,119 нм, ионные радиусы Вr — (6), Br 3+ (4), Br 5+ (3), Br 7+ (6X Вг 7+ (4) соотв. 0,182, 0,073, 0,045, 0,053, 0,039 нм (в скобках указано координац. число).
Молекула брома двухатомна (в парах обнаружены молекулы Вr4), длина связи в молекуле 0,228 нм; энергия диссоциации 190,0 кДж/моль, степень диссоциации 0,16% при 800°С и 18,3% при 1284°С
Содержание брома в земной коре 1,6*10 -4 % по массе (10 15 -10 16 т). Собственно минералы бромаргирит AgBr и эмболит Ag(Cl, Br) редки. Бром находится в природе в рассеянном состоянии, являясь постоянным спутником хлора. Соли брома легко выщелачиваются и накапливаются в морской воде (0,065% по массе), рассолах соляных озер (до 0,2%) и в подземных рассолах (до 0,1%), обычно связанных с соляными и нефтяными месторождениями. В виде изоморфной примеси бром содержится в поваренной соли NaCl (0,005-0,03% по массе), сильвине КС1 (0,02-0,1%), карналлите КМgС13*6Н2О (0,1-0,39), бишофите MgCl2*6H2O (до 0,6%).
Свойства. При обычных условиях бром — тяжелая жидкость с резким запахом, в отраженном свете темно-фиолетового, почти черного цвета, в проходящем — темно-красного; легко образует желто-бурые пары; т. пл. — 7,25 °С, т. кип. 59,2 °С. Твердый бром — красно-коричневые игольчатые кристаллы со слабым металлич. блеском, к-рые при — 252 °С становятся бесцветными. Бром кристаллизуется в ромбич. системе, а = = 0,448 нм, b = 0,667 нм, с = 0,872 нм, z = 4, пространств. группа Сета. Плотн, твердого брома 4,073 г/см 3 ( — 7,3 °С), жидкого — 3,1055 г/см 3 (25°С); tкрит 315°С, ркрит 10,0 МПа, dкрит 1,26 г/см 3 ; ур-ние температурной зависимости давления пара над жидким бромом: lgp(Ha) = -2047,75/T — 0,0061007 + 0,9589*lg T+ 10,76568; С°р 75,69 Дж/(моль*К); 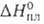
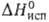
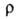
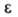
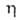
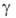
Бром раств. в воде (3,58 г в 100 г при 20 °С), в присут. хлоридов и особенно бромидов р-римостъ повышается, а в присут. сульфатов понижается; ниже 5,84°С из водных р-ров осаждаются гранатово-красные кристаллы октагидрата. Р-римость воды в жидком броме составляет 0,05% по массе. В водных р-рах бром частично гидролизуется: Вг2 + Н2О_Н + + Вг — + НВrO; константа равновесия Кр = 5,8*10 -9 (25°С). Насыщенный водный р-р брома в воде наз. бромной водой. В конц. H2SO4 и Н3РО4 бром раств. слабо. В р-рах щелочей на холоду образует бромид и гипобромит соответствующего металла, а при повышенных т-рах — бромид и бромат. Бром смешивается во всех отношениях с большинством орг. р-рителей.
По реакц. способности бром занимает промежут. положение между С12 и 12. С др. галогенами образует неустойчивые BrF3 (т. пл. 8,8°С, т. кип. 127 °С), BrF5 (т. пл.-61,3°С, т. кип. 40,5°С), BrCl (т. пл. ок.-66°С, т. кип. ок.-5°С с разл.) и IBr (т. пл. 41 °С, т. кип. 116°С), отличающиеся высокой хим. активностью (см. Межгалогенные соединения). С О2 и N2 бром непосредственно не реагирует даже при повышенных т-рах, его нестойкие соед. с этими элементами (Вr2О, ВгО2, Br3O8, NBr3*6NH3) получают косвенными методами. Бром не реагирует также с углеродом. При взаимод. с S, Se, Те, Р, As и Sb образуются соответствующие бромиды: S2Br2, РВr3, РВr5, неустойчивые SeBr4 и Se2Br2, TeBr4, AsBr3, SbBr3. Бор и Si образуют с бромом при нагревании ВВг3 и SiBr4.
Нек-рые металлы (напр., К, А1) энергично взаимод. с сухим бромом, но в большинстве случаев из-за образования на пов-сти защитной пленки бромида, нерастворимого в броме, р-ция энергично идет только в присут. воды, растворяющей пленку. Стойки к действию брома Pt и Та, в меньшей степени — Ag, Pb и Ti. С Н2 при нагр. бром образует бромистый водород.
Бром — сильный окислитель, он окисляет в водных р-рах I — до I, сульфиты и тиосульфаты — до сульфатов, нитриты — до нитратов, NH3 до N2. Ион Вr — в водных р-рах бромидов окисляется С12, КМnО4, К2Сr2О7, Н2О2 до Вr2. Из р-ций брома с орг. соед. Наиб. характерны присоединение по кратным связям и замещение водорода (обычно в присут. кат. или при действии света). Ниже приводятся сведения о нек-рых соед. брома.
Бром образует ряд кислородсодержащих к-т. Бромноватистая к-та НВгО существует только в разбавл. водных р-рах; является слабой к-той (рКа 8,69); сильный окислитель; при стоянии диспропорционирует на НВr и НВrО3, в присут. кат. (Pt, Fe) или под действием света разлагается с выделением О2; получают гидролизом Вr2.
Бромистая к-та НВгО2 существует только в водных р-рах; в течение 4 ч полностью разлагается; м.б. получена взаимод. AgNO3 с Вг2 в воде. Бромноватая к-та НВrO3 существует только в водных р-рах, к-рые м. б. сконцентрированы в вакууме до концентрации 50%; при стоянии и нагревании разлагается; сильная к-та, окислитель; получают при окислении брома хлором в воде или разложением Ва(ВrО3)2 серной к-той. Бромная к-та НВrO4 известна в водных р-рах, к-рые можно сконцентрировать в вакууме до концентрации 80%; при нагр. разлагается; сильная к-та; в конц. р-рах сильный окислитель; м.б. получена пропусканием р-ра КВrO4 через Н + -катионит.
Соли НВrO3 (броматы) — бесцв. кристаллы; устойчивы при обычных условиях; броматы щелочных металлов разлагаются при нагр. по схеме МВгО3 -> МВr + 1,5О2, др. металлов — по схеме М(ВrO3)2 -> МО + Вr2 + 2,5О2. Для NaBrO3 т. пл. 380°С; плотн. 3,34 г/см 3 ; р-римость в воде (г в 100г)-36,4 (20°С), 90,8 (100°С). Для КВrO3 плотн. 3,25 г/см 3 ; разлагается при 400°С; р-римость в воде (г в 100 г)-6,9 (20°С), 49,7 (100°С). Броматы Na и К получают электрохим. или хим. (действием С12) окислением NaBr или КВr, а также взаимод. брома с NaOH или КОН. Применяются в броматометрии. Ва(ВrO3)2 кристаллизуется из водных р-ров в виде дигидрата; раств. в воде (0,657 г безводной соли в 100 г при 20 °С); получают обменной р-цией броматов щелочных металлов с BaCl; используется для получения НВrO3.
Соли НВrO4 (п е р б р о м а т ы) — кристаллы, стабильны в обычных условиях, выше 250°С разлагаются (напр., 2КВrO4 -> О2 + 2КВrO3); хорошо раств. в воде; умеренные окислители; получают окислением броматов Na или К фтором в щелочной среде.
Известны оксифториды брома — сильные окислители и фторирующие агенты. Пербромилфторид (триоксимонофторид брома) ВгО3F — бесцв. газ; т. пл.-110,35°С, т. кип. 2,35°С; плотн. жидкости 2,2 г/см 3 ; ур-ние температурной зависимости давления пара: lgp (мм рт. ст.) = 17,6986 — -3048,45/Т (188-292 К);
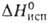
Бромилфторид (диоксомонофторид брома) ВrO2F — бесцв. летучая жидкость; т. пл. — 9°С; для газа С° 62,898 Дж/(моль*К), S°298 294,11 Дж/(моль-К). Выше 52°С разлагается на BrF3, Вr2 и О2. В воде бурно гидролизуется до НВrO3 и HF. С фторидами щелочных металлов дает соли с анионом ВrO2F2 — , с сильными к-тами Льюиса — соли с катионом бромила, напр. BrO2 + SbF6 — . Получают р-цией BrF5 с КВrO3 в жидком HF или гидролизом BrF5 при низких т-рах.
Окситрифторид брома (бромозил трифторид) ВrOF3 — бесцв. жидкость; т. пл. ок. 0°С, при 25°С давление пара 6,65 Па. При комнатной т-ре медленно разлагается на BrF3 и О2. С донорами иона F — дает устойчивые кристаллич. соли типа K + BrOF4, с акцепторами F — — соли с катионом OBrFI, напр. OBrF2 + AsF6 — . Получают реакцией O2AsF6 с KBrOF4 или действием KrF2 на BrO2F.
Получение. Для получения брома используют морскую воду, озерные и подземные рассолы, а также щелока калийного произ-ва (концентрация брома до 4-5 кг/м 3 ), содержащие бром в виде Вr — . Бром выделяют пропусканием С12 с послед. отгонкой с водяным паром (при концентрации брома в р-ре более 1 кг/м 3 ) или воздухом в насадочных колоннах из керамики, стекла или Ti. Р-ры, имеющие щелочную р-цию, предварительно подкисляют (обычно H2SO4) до рН 2,5-3,0. В верхнюю часть колонны подается подогретый реакционный р-р, снизу — водяной пар и неск. выше — С12. Пары, выходящие из колонны, конденсируют. Далее бром отделяют от воды и очищают от примесей С12 и орг. соед. ректификацией. Применение воздуха вместо водяного пара позволяет использовать р-ры с содержанием брома менее 1 кг/м 3 . Р-р после обработки С12 подают в верхнюю часть колонны, снизу -воздух. Из образовавшейся бромвоздушной смеси бром улавливают р-ром FeBr2; получаемый при этом FeBr3 восстанавливают железными стружками до FeBr2. По др. способу к бромовоздушной смеси добавляют SO2, к-рый в присут. паров воды образует с бромом смесь НВг и H2SO4; бром выделяют действием С12. Для поглощения брома могут быть использованы р-ры NaOH или Na2CO3 (3Na2CO3 + 3Br2 = 5NaBr + NaBrO3 + ЗСО2). В этом случае бром выделяют действием H2SO4. Остаточный бром в отработанных р-рах обезвреживают Na2S2O3.
Определение. Качественно бром обнаруживают по красно-фиолетовому окрашиванию фуксина, розовому — эозина, желтому — слоя орг. р-рителя (напр., СС14), а также р-цией с флуоресцеином. Количеств. анализ осуществляют иодометрически, аргентометрически, меркуриметрически, а также потенциометрич. титрованием.
Применение. Бром используют для получения бромсодержащих неорг. (напр., NaBr, КВг, НВг) и орг. соед. (ок. половины производимого Вr2 — в произ-ве С2Н4Вr2), бром и бромную воду применяют в аналит. химии, напр. для кулонометрич. определения As 3+ , Sb 3+ , V 4+ , а также для качеств. и количеств, анализа орг. соединений.
Мировое произ-во брома (без СССР) ок. 300 тыс. т/год (1980). Главные производители: США, СССР, Великобритания, Израиль, Франция, ГДР, ФРГ, Италия.
Бром ядовит. При работе с ним пользуются противогазом, перчатками и спецодеждой. При содержании брома в воздухе ок. 0,001% наблюдаются раздражение слизистых оболочек, головокружение, кровотечение из носа, при 0,02% — удушье, спазмы и заболевание дыхат. путей. ПДК 0,5 мг/м 3 . Попадание жидкого брома на кожу вызывает зуд, при длительном действии образуются медленно заживающие язвы. При отравлении бромом пострадавшего нужно вывести на свежий воздух, дать теплое молоко с содой. Кожа, обожженная бромом, промывается многократно водой и р-ром Na2CO3, смазывается мазью, содержащей NaHCO3. Бром открыт в 1826 Ж. Баларом.
===
Исп. литература для статьи «БРОМ» : Позин М. Е., Технология минеральных солей, 4 изд., ч. 1, Л., 1974, с. 206-36; Ксензенко В. И., Стасиневич Д. С, Химия и технология брома, иода и их соединений, М., 1979: Егоров Л. Ф., Осыка В. Г., Пивоваров М. Д., Технология получения бромжелеза из природных рассолов, М., 1979; Полянский Н. Г., Аналитическая химия брома, М., 1980; Bromine and its compounds, ed. by Z.E. Jolles, L., 1966; Comprehensive inorganic chemistry, v. 2, Oxf., 1973. В. И. Ксензенко, Ц. С. Стасиневич.
Страница «БРОМ» подготовлена по материалам химической энциклопедии.
Источник