Соль мора имеет формулу fe
Соль мора имеет формулу Fe(NH4)2(so4)2×6h2o вфчисли масовую долю:азота водорода кислорода воды
Трудности с пониманием предмета? Готовишься к экзаменам, ОГЭ или ЕГЭ?
Воспользуйся формой подбора репетитора и занимайся онлайн. Пробный урок — бесплатно!
- bookmark_border
- 22.09.2017 10:19
- Химия
- remove_red_eye 16311
- thumb_up 34
Ответы и объяснения 1
Mr(Fe(NH4)2(SO4)2*6H2O) = 56+2*14+8*1+2*32+8*16+12*1+6*16=392
W(N)=28/392=0.07=7%
W(H2O)=108/392=0.276=27.6%
W(SO4)=192/392=0.49=49%
как то так
Знаете ответ? Поделитесь им!
Как написать хороший ответ?
Чтобы добавить хороший ответ необходимо:
- Отвечать достоверно на те вопросы, на которые знаете правильный ответ;
- Писать подробно, чтобы ответ был исчерпывающий и не побуждал на дополнительные вопросы к нему;
- Писать без грамматических, орфографических и пунктуационных ошибок.
- Копировать ответы со сторонних ресурсов. Хорошо ценятся уникальные и личные объяснения;
- Отвечать не по сути: «Подумай сам(а)», «Легкотня», «Не знаю» и так далее;
- Использовать мат — это неуважительно по отношению к пользователям;
- Писать в ВЕРХНЕМ РЕГИСТРЕ.
Есть сомнения?
Не нашли подходящего ответа на вопрос или ответ отсутствует? Воспользуйтесь поиском по сайту, чтобы найти все ответы на похожие вопросы в разделе Химия.
Трудности с домашними заданиями? Не стесняйтесь попросить о помощи — смело задавайте вопросы!
Химия — одна из важнейших и обширных областей естествознания, наука о веществах, их составе и строении, их свойствах, зависящих от состава и строения, их превращениях, ведущих к изменению состава — химических реакциях, а также о законах и закономерностях, которым эти превращения подчиняются.
Источник
Соль Мора
Сульфат аммония-железа (II) (соль Мора) — неорганическое соединение, двойная сернокислая соль железа и аммония с формулой Fe(NH4)2(SO4)2.
Свойства
Химическая формула: FeSO4·(NH4)2SO4·6H2O (или Fe(NH4)2(SO4)2·6H2O). Представляет собой неярко сине-зелёные моноклинные кристаллы. Растворяется в воде. Растворимость соли Мора в воде равна 21,6 г безводного вещества в 100 г воды при 20 °C. В кислоте растворимость несколько больше. Устойчива на воздухе. Парамагнетик. Соль Мора используется в медицине (добавляется в пищу, или в виде фармакопейного препарата, при нехватке в организме больного железа), для определения уробилина, в фармацевтике.
Применение
Соль Мора применяется в научно-исследовательских работах и химических лабораториях как удобная форма препарата железа (II): для определения концентрации (титра) перманганата калия в растворах, при определении концентраций хрома и ванадия в растворах этилового спирта и эфира. В растворах ион Fe 2+ даже слабыми окислителями легко окисляется до Fe 3+ .
Также, в виде концентрированных растворов, применяется для пропитки древесины для защиты её от гниения. Имеет и другие применения.
Соль названа в честь немецкого химика Карла Фридриха Мора (1809—1879).
- Алюминат железа II ( Fe(AlO2)2 ) Алюминат железа II
- Арсенат железа II (Fe3(AsO4)2) Железо мышьяковокислое
- Арсенат железа III (FeAsO4) Мышьяковокислое железо
- Ацетат железа II (Fe(CH3COO)2) Железо уксуснокислое
- Ацетат железа III (Fe(CH3COO)3) Уксуснокислое железо
- Берлинская лазурь () Прусская Синь
- Бромид железа II (FeBr2) Бромистое железо
- Бромид железа III (FeBr3) Трибромид железа
- Бромид железа II,III (Fe3Br8) Железо бромистое
- Ванадат железа III (FeVO4) Железо ванадиевокислое
- Вольфрамат железа II (FeWO4) Железо вольфрамовокислое
- Гексаплутонийжелезо (FePu6) Гексаплутонийжелезо
- Гексахлороплатинат IV железа (Fe[PtCl6]) Гексахлороплатеат железа
- Гексацианоферрат II железа II (Fe2[Fe(CN)6]) Гексацианоферрат железа II
- Гексацианоферрат II железа III (Fe4[Fe(CN)6]3) Гексацианоферрат железа III
- Гексацианоферрат III железа II,III (Fe III 4Fe II 3[Fe(CN)6]6) Гексацианоферрат железа II,III
- Гексацианоферрат III железа II (Fe3[Fe(CN)6]2) Турнбулева синь
- Гексацианоферрат II калия (K4[Fe(CN)6]) Желтая кровяная соль
- Гексацианоферрат III калия (K3[Fe(CN)6]) Красная кровяная соль
- Гидроксид железа II (Fe(OH)2) Гидроксид железа II
- Гидроксид железа III (Fe(OH)3) Гидроксид железа III
- Динитрозилдикарбонилжелезо (Fe(CO)2(NO)2) Динитрозилдикарбонилжелезо
- Дипразеодимгептадекажелезо (Fe17Pr2) Гептадекажелезодипразеодим
- Диренийтрижелезо (Fe3Re2) Трижелезодирений
- Дисамарийгептадекажелезо (Fe17Sm2) Гептадекажелезодисамарий
- Диселенид железа (FeSe2) Железо селенистое
- Дисилицид железа (FeSi2) Железо кремнистое
- Дистаннид железа (FeSn2) Дистаннид железа
- Дистаннид трижелеза (Fe3Sn2) Дистаннид трижелеза
- Дисульфид железа II (FeS2) Дисульфид железа
- Дителлурид железа (FeTe2) Дителлурид железа
- Дихромат железа III (Fe2(Cr2O7)3) Хромовокислое железо
- Додекакарбонилтрижелезо (Fe3(CO)12) Додекакарбонилтрижелезо
- Железо (Fe)
- Железистосинеродистая кислота (H4[Fe(CN)6]) Кислота железистосинеродистая
- Железониобий (FeNb) Железониобий
- Железосинеродистая кислота (H3[Fe(CN)6]) Кислота железосинеродистая
- Йодид железа II,III (Fe3I8) Йодистое железо
- Йодид железа II (FeI2) Железо йодистое
- Карбонат железа II (FeCO3) Железо углекислое
- Лактат железа II (Fe(C3H5O3)2) Железо молочнокислое
- Лактат железа III (Fe(C3H5O3)3) Молочнокислое железо
- Метаванадат железа III (Fe(VO3)3) Ванадиевокислое железо
- Метагидроксид железа (FeO(OH)) Железо метагидроксид
- Молибдат железа II (FeMoO4) Железо молибденовокислое
- Нитрат железа II (Fe(NO3)2) Железо азотнокислое
- Нитрат железа III (Fe(NO3)3) Азотнокислое железо
- Нитрид дижелеза (Fe2N) Железо азотистое
- Оксалат железа II (FeC2O4) Железо щавелевокислое
- Оксид железа II (FeO) Оксид железа
- Оксид железа III (Fe2O3) Окись железа ( Железный сурик )
- Оксид железа II,III (Fe3O4) Закись-окись железа
- Оксихлорид железа (FeOCl) Оксид-хлорид железа
- Пентакарбонилжелезо ([Fe(CO)5]) Пентакарбонил железа
- Перхлорат железа II (Fe(ClO4)2) Железо хлорнокислое
- Пирофосфат железа III (Fe4(P2O7)3) Железо пирофосфорнокислое
- Пирофосфат железа III-натрия (FeNaP2O7) Фосфорнокислое железо-натрий
- Платинажелезо (FePt) Железоплатина
- Плутонийдижелезо (Fe2Pu) Плутонийдижелезо
- Празеодимдижелезо (Fe2Pr) Дижелезопразеодим
- Ржавчина
- Самарийдижелезо (Fe2Sm) Дижелезосамарий
- Самарийпентажелезо (Fe5Sm) Пентажелезосамарий
- Самарийтрижелезо (Fe3Sm) Трижелезосамарий
- Селенид железа II (FeSe) Селенистое железо
- Силикат железа II (FeSiO3) Железо кремнекислое
- Силицид дижелеза (Fe2Si) Кремнистое железо
- Силицид железа (FeSi)
- Соль Мора (FeSO4·(NH4)2SO4·6H2O) Сульфат аммония-железа II
- Станнид железа (FeSn)
- Станнид трижелеза (Fe3Sn)
- Сульфат железа (FeSO4) Железо сернокислое (Железный купорос)
- Сульфат железа II-калия (K2Fe(SO4)2) Сернокислое железо-калий
- Сульфат железа III (Fe2(SO4)3) Железо сернокислое III
- Сульфат железа III-аммония (NH4Fe(SO4)2·12H2O) Сернокислое железо-аммоний
- Сульфат железа III-калия (KFe(SO4)2) Сернокислое железо-калий
- Сульфид железа II,III (Fe3S4)
- Сульфид железа II (FeS)
- Сульфид железа II-меди II (CuFeS2)
- Сульфид железа III (Fe2S3)
- Сульфид железа III-калия (KFeS2) Сернистое железо-калий
- Сульфит железа II (FeSO3) Железо сернистокислое
- Танталат железа II (Fe(TaO3)2) Железо танталовокислое
- Тартрат железа II (FeC4H4O6) Железо виннокислое
- Теллурид железа II (FeTe) Железо теллуристое
- Теллурид железа III (Fe2Te3) Теллуристое железо
- Тетракарбонилдигидриджелезо (H2Fe(CO)4)
- Тетракарбонилжелезо (Fe(CO)4) Тетракарбонил железа
- Тиосульфат железа II (FeSO3S) Тиосернокислое железо
- Тиоцианат железа II (Fe(SCN)2) Железо роданистое
- Тиоцианат железа III (Fe(SCN)3) Тиоциановокислое железо
- Титанат железа II (FeTiO3) Титановокислое железо
- Триренийдижелезо (Fe2Re3) Дижелезотрирений
- Формиат железа III (Fe(CHO2)3) Железо муравьинокислое
- Фосфат железа II (Fe3(PO4)2) Железо фосфорнокислое
- Фосфат железа III (FePO4) Фосфорнокислое железо
- Фосфинат железа III (Fe(PH2O2)3) Железо фосфорноватистокислое ( гипофосфит железа )
- Фторид железа II (FeF2) Железо фтористое
- Фторид железа III (FeF3) Фтористое железо
- Хлорид железо II (FeCl2) Железо двухлористое
- Хлорид железа III (FeCl3) Железо треххлористое
- Хлорид железа II,III (Fe3Cl8) Хлористое железо II,III
- Хлорид железа III-калия (FeCl3•2KCl•H2O) Хлористое железо-калий
- Хромат железа III (Fe2(CrO4)3) Железо хромовокислое
- Хромит железа II (Fe(СrO2)2) тетраоксид железа-дихрома
- Цианид железа II (Fe(CN)2) Железо цианистое
- Цитрат железа II (FeC6H6O7) Железо лимоннокислое
- Цитрат железа III (FeC6H5O7) Лимоннокислое железо
- Цитрат железа III-аммония (Fe(NH4)3(C6H5O7)2) Лимоннокислое железо-аммоний
Источник
Соль мора имеет формулу fe
Соль Мора имеет формулу Fe(NH4)2(SO4)2 6H2O. Вычислите в этом веществе массовую долю : а) азота, б) воды, в) сульфат-ионов.
Трудности с пониманием предмета? Готовишься к экзаменам, ОГЭ или ЕГЭ?
Воспользуйся формой подбора репетитора и занимайся онлайн. Пробный урок — бесплатно!
- bookmark_border
- 06.10.2017 13:52
- Химия
- remove_red_eye 19714
- thumb_up 38
Ответы и объяснения 1
Знаете ответ? Поделитесь им!
Как написать хороший ответ?
Чтобы добавить хороший ответ необходимо:
- Отвечать достоверно на те вопросы, на которые знаете правильный ответ;
- Писать подробно, чтобы ответ был исчерпывающий и не побуждал на дополнительные вопросы к нему;
- Писать без грамматических, орфографических и пунктуационных ошибок.
- Копировать ответы со сторонних ресурсов. Хорошо ценятся уникальные и личные объяснения;
- Отвечать не по сути: «Подумай сам(а)», «Легкотня», «Не знаю» и так далее;
- Использовать мат — это неуважительно по отношению к пользователям;
- Писать в ВЕРХНЕМ РЕГИСТРЕ.
Есть сомнения?
Не нашли подходящего ответа на вопрос или ответ отсутствует? Воспользуйтесь поиском по сайту, чтобы найти все ответы на похожие вопросы в разделе Химия.
Трудности с домашними заданиями? Не стесняйтесь попросить о помощи — смело задавайте вопросы!
Химия — одна из важнейших и обширных областей естествознания, наука о веществах, их составе и строении, их свойствах, зависящих от состава и строения, их превращениях, ведущих к изменению состава — химических реакциях, а также о законах и закономерностях, которым эти превращения подчиняются.
Источник
Сульфат железа (II) аммония — Ammonium iron(II) sulfate
Сульфат железа (II) аммония или соль Мора — это неорганическое соединение с формула (NH 4)2Fe (SO 4)2(H2O)6. Содержит два разных катиона s, Fe и NH 4, он классифицируется как двойная соль сульфата железа и сульфата аммония. Это обычный лабораторный реагент, поскольку он легко кристаллизируется, а кристаллы устойчивы к окислению воздухом. Как и другие соли сульфата двухвалентного железа, сульфат двухвалентного аммония растворяется в воде с образованием акво-комплекса [Fe (H 2O)6], который имеет октаэдрическую молекулярную геометрию. Его минеральная форма морит.
- 1 Структура
- 2 Области применения
- 3 Получение
- 4 Загрязняющие вещества
- 5 Ссылки
Структура
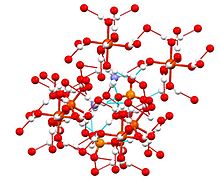
Это соединение является членом группы двойных сульфатов, называемых шёнитами или солями Туттона. Соли Туттона образуют моноклинные кристаллы и имеют формулу M 2 N (SO 4)26H2O (M = различные монокатионы). Что касается связывания кристаллы состоят из октаэдров [Fe (H 2O)6] центров, которые связаны водородными связями с сульфатом и аммонием.
Структура сульфата двухвалентного аммония с сеткой водородных связей выделена ( N — фиолетовый, O — красный; S — оранжевый, Fe = большой красный).
Соль Мора названа в честь немецкого химика Карла Фридриха Мора, который добился многих важных успехов в методологии титрования в 19 век.
Применения
В аналитической химии эта соль является предпочтительным источником ионов двухвалентного железа, поскольку твердое вещество имеет длительный срок хранения и устойчиво к окислению. Эта стабильность в некоторой степени распространяется на растворы, отражающие влияние pH на окислительно-восстановительную пару двухвалентное / трехвалентное железо. Это окисление легче происходит при высоком pH. Ионы аммония делают растворы соли Мора слабокислыми, что замедляет этот процесс окисления. Серную кислоту обычно добавляют в растворы для уменьшения окисления до трехвалентного железа.
Он используется для измерения высоких доз гамма-излучения.
Получение
Соль Мора получают растворением эквимолярной смеси гидратированных сульфат железа и сульфат аммония в воде, содержащей небольшое количество серной кислоты, а затем подвергание полученного раствора кристаллизации. Сульфат двухвалентного аммония образует светло-зеленые кристаллы. Эта соль при нагревании ионизируется с образованием всех присутствующих в ней катионов и анионов.
Загрязняющие вещества
Обычные примеси включают магний, никель, марганец, свинец и цинк, многие из которых образуют изоморфные соли.
Источник