- Извлечение сырьевых ресурсов из морской воды
- Технология добычи каких химических элементов из морской воды отработана и экономически оправдана уже сегодня?
- Химические ресурсы Мирового океана
- Перспектива добычи золота и других ценных элементов
- Химические ресурсы мирового океана и их добыча из морской воды
- Химические ресурсы мирового океана и их добыча из морской воды.
- Химические ресурсы мирового океана и их добыча из морской воды:
Извлечение сырьевых ресурсов из морской воды
Океан является огромной кладовой химических веществ. В каждой кубической миле морской воды содержится 1,5 -1011 кг растворенных твердых веществ. Океан столь огромен, что если концентрация какого-либо вещества в морской воде составляет всего 1 миллиардную долю по весу, то его содержание в мировом океане исчисляется в 5-109 кг. Тем не менее океан еще мало используется как источник сырьевых материалов, поскольку стоимость извлечения необходимых веществ из воды слишком высока. Лишь три вещества получают из морской воды в промышленно широких масштабах: хлорид натрия, бром и магний.
ХЛОРИД НАТРИЯ
Поскольку хлорид натрия-самое распространенное вещество из числа растворенных в морской воде, нет ничего удивительного в том, что значительное количество (приблизительно 4.1010кг ежегодно) чистого хлорида натрия получают из морской воды. С этой целью морскую воду фильтруют и затем дают ей испаряться до тех пор, пока концентрация содержащегося в ней NaCl не превысит его растворимости. Твердый NaCl, который выкристаллизовывается из морской воды, оказывается довольно чистым, но его можно перекристаллизовывать из пресной воды до еще более высокой степени чистоты в зависимости от дальнейшего использования.
БРОМ
Ежегодно во всем мире получают более 2,3 • 108 кг брома, главным образом из морской воды. Концентрация бромид-иона в морской воде составляет всего 8,3.10 –4 М. На первой стадии извлечения брома из морской воды к ней добавляют серную кислоту, что снижает рН до 3,5. Затем через подкисленную воду продувают газообразный хлор в некотором избытке по сравнению с содержащимся в ней бромом. Между растворенным в воде газообразным хлором и бромид-ионом протекает окислительно-восстановительная реакция:
С12(водн.) + 2Вr(водн.) = Вr2(водн.) + 2С1(водн.)
Для выделения брома из морской воды ее пропускают через специальную башню, выложенную брусками дерева; в обратном направлении через башню продувают воздух. Для выделения брома из потока прошедшего через башню воздуха его обрабатывают сернистым ангидридом SO2 и паром. В результате образуются бромистоводородная и серная кислоты:
SO2(r.) + Вr2(г.) + 2Н2О(ж.) = 2НВr(водн.) + Н2SО4(водн.)
Чтобы извлечь бром из этого раствора, его снова обрабатывают надлежащим количеством хлора и затем удаляют бром, продувая воздухом. После этого смесь газообразного брома с воздухом пропускают над холодной поверхностью. Температура кипения жидкого брома составляет 59°С, что позволяет отделять его от воды перегонкой. Разбавленная серная кислота, остающаяся после удаления брома, используется для подкисления свежей порции впускаемой морской воды.
МАГНИЙ
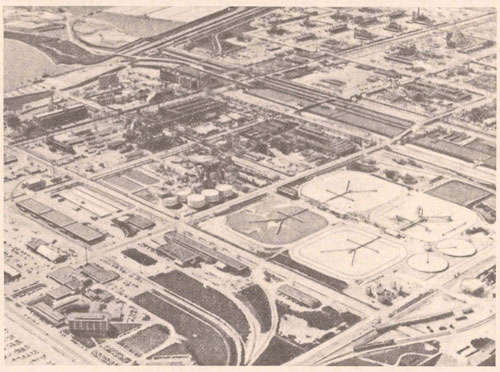
Магний-второй по содержанию металлический элемент в морской воде. Самый большой завод для получения магния из морской воды в США принадлежит компании «Доу Кемикл» и находится в г. Фрипорте (штатт Техас). На этом заводе Mg2+ осаждают из морской воды в больших отстойниках (рис.1) в виде Mg(OH)2 (ПР = = 1,8.10 -11) путем добавления к морской воде негашеной извести СаО.
Рис. 1. Вид сверху на отстойники (в центре) для осаждения гидроокиси магния из морской воды на заводах компании «Доу Кемикл» (США). Рисунок из книги Т. Брауна “Химия в центре наук”, М, Мир, 1983
Оксид кальция для данного процесса в свою очередь получают из раковин моллюсков. Раковины моллюсков состоят из карбоната кальция. Их промывают, затем прокаливают в специальной обжиговой печи и таким образом получают негашеную известь:
Гидроксид магния получают по реакции:
Мg2+(водн.) + СаО(тв.) + Н2О(ж.) = Мg(ОН)2(тв.) + Са2+(водн.)
Осаждающийся гидроксид магния содержит примеси ионов Са2+, Na+ и HCO3. Твердый осадок отфильтровывают и затем обрабатывают смесью растворов НС1 и H2SO4. В кислом растворе происходит растворение Mg(OH)2
Mg(OH)2(тв.) + 2Н+(водн.) = Мg2+(водн.) + 2Н2О(ж.)
Большая часть примесных ионов натрия кристаллизуется в составе NaCl, а ион кальция осаждается в составе CaSO4. Раствор, содержащий ионы Mg2+, отфильтровывают и затем концентрируют в испарителе. Таким образом, в конце концов получают твердый MgCl2. Его растворяют в смеси расплавленных хлоридов металлов при 700°С в электролизных установках (см. рис. 2). Электрическая энергия, подводимая к электролизерам, расходуется на образование из расплавленного хлорида магния металлического магния и газообразного хлора:
электроэнергия
МgС12(ж.) = Мg(ж.) + С12(г.)
Расплавленный металл отливают в слитки, которые имеют чистоту 99,9%.
Рис. 2. Установки для электролитического получения Mg из MgCl2 на заводе компании «Доу Кемикл» (США). Круглые вертикальные стержни представляют собой угольные аноды, а стержни прямоугольного сечения — медные проводники, по которым в электролизеры подается ток силой до 100000 ампер. Рисунок из книги Т. Брауна “Химия в центре наук”, М, Мир, 1983
Источник
Технология добычи каких химических элементов из морской воды отработана и экономически оправдана уже сегодня?
Технология добычи каких химических элементов из морской воды отработана и экономически оправдана уже сегодня?
Думаю, в будущем человечество найдет способ получения того богатства, что содержится в морской воде, а пока, как говорится, не густо. 🙁 Вопрос интересный, и я с удовольствием расскажу о том, добыча каких элементов показала свою эффективность уже сегодня и, конечно, о том, каков потенциал обычной морской воды.
Химические ресурсы Мирового океана
Несмотря на то огромное разнообразие элементов, что содержат его воды, в наши дни извлекается самая малая часть, хотя многие так необходимы человечеству. Все дело в том, что пока не удалось выработать методы, которые будут достаточно эффективны. Извлекаются лишь те элементы, добыча которых обходится значительно дешевле, чем на суше, например:
Сложность процесса и эффективность зависят от концентрации вещества в воде. К примеру, добыча обычной соли обусловлена сравнительной экономичностью и простотой получения ввиду достаточной концентрации. Ее выпаривают, а иногда просто вырубают из естественных отложений как в природных, так и искусственных бассейнах. В общей сложности, из 1 тысячи кубометров раствора получают до полутора тонн готового к употреблению продукта.
Перспектива добычи золота и других ценных элементов
Золотоносность вод океана окончательно не установлена, однако известно, что 1 тонна воды содержит минимум 5 миллиграммов металла. Установлено, в каких состояниях пребывает элемент, но вот в чем вопрос: как его эффективно извлечь? Применялись различные способы, например, буксировка специальных пиритовых улавливателей за судном, сепарация при помощи свинцовой стружки, однако все это оказалось нерентабельно. Что касается других элементов, то запасы их просто огромны: даже при условии минимальной концентрации, 1 км³ воды может содержать:
- до 20 млн тонн соли;
- до 11 млн тонн магния;
- до 0,7 млн тонн серы;
- 8 тонн алюминия;
- 2 тонны урана и 250 кг серебра.
Потенциал Мирового океана легко увидеть на примере урана, запасы которого в его водах оцениваются в 5 млрд тонн против 4 млн на всей суше.
Источник
Химические ресурсы мирового океана и их добыча из морской воды
Химические ресурсы мирового океана и их добыча из морской воды.
Мировой океан обладает колоссальными химическими ресурсами, которые могут быть извлечены из него попутно – при опреснении морской воды с целью получения питьевой воды.
Химические ресурсы мирового океана и их добыча из морской воды:
В морской воде в виде солей растворены практически все химические элементы из таблицы Д.И. Менделеева . Из 118 известных химических элементов 70 найдено в океанских и морских водах. По сути, мировой океан содержит неисчерпаемые запасы нужных и важных для человека химических элементов, правда, в малых концентрациях.
Например, содержание иридия в океане 5,0×10 -9 %, серебра – 1,0×10 -8 %, германия – 6,0×10 -9 %, меди – 3,0×10 -7 %, кобальта – 8,0×10 -9 %, никеля – 2,0×10 -7 %, золота – 5,0×10 -9 %, урана – 3,3×10 -7 %, алюминия – 5,0×10 -7 %, рубидия – 0,000012 %.
Учитывая громадный объем вод Мирового океана, суммарное количество растворенных в нем химических элементов и их соединений исчисляется колоссальными величинами. Общая масса химических ресурсов океана равна 50х10 15 тонн.
В настоящее время не все химические элементы извлекаются из вод мирового океана, а только те, добыча которых рентабельна. На сегодня наиболее экономически обоснована добыча из морской воды соли поваренной (третья часть мировой добычи), брома (около 70% всей добычи), магния (свыше 61% мировой добычи) и калия .
Другие химические элементы могут быть добыты из морской воды попутно. Так, при опреснении морской воды с целью получения пресной питьевой воды остается осадок. Химические элементы могут быть извлечены из него и использованы в дальнейшем.
Примечание: © Фото https://www.pexels.com, https://pixabay.com
ориентация на ресурсы сибирской химической базы химической промышленности
уральские горно химические природные минеральные ресурсы страны примеры и государства
возобновляемые горно химические ресурсы мирового океана примеры россии
природные ресурсы центральной химической базы
ооо химический ресурс санкт петербург калуга
страны богатые химическими ресурсами
энергетические трудовые ресурсы химических лабораторий химического производства в химической технологии
назовите месторождения технологических и химических ресурсов
Источник