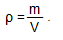Калькулятор плотности пресной и соленой воды
Плотность воды — величина, которая определяется как отношение массы жидкости к ее объему. В зависимости от состава воды ее плотность может значительно различаться.
Морская вода
Морская вода содержит в своем составе разные минералы, в том числе магний, марганец, золото, медь и даже уран. Но не только сама вода отличается таким минерализованным составом. Морские жители — это основной источник минералов для воды. Ламинарии накапливают йод, моллюски — медь, радиолярии — стронций, асцидии — ванадий, а медузы — олово, цинк и свинец. В результате разложения подводных жителей морская вода получает минералы, которые затем накапливают новые поколения ламинарий или радиолярий. Такой дикий минеральный состав делает морскую воду непригодной для питья, ведь для выведения химических элементов из организма потребуется больше воды, чем ее выпитое количество.
Соленость
Если попробовать морскую воду на вкус, то она кажется горько-соленой. На 1 литр морской воды приходится в среднем 25 грамм хлорида натрия, а горечь ей придают 3,8 г хлористого магния и 1,7 г сернокислого магния. В целом в морской воде содержится около 35 г различных солей, благодаря чему ее плотность всегда выше, чем у пресной. Соленость воды выражается в промилле. Фраза «соленость 16 ‰» эквивалентна записи «соленость 16 PSU» или «соленость 1,6%». Это означает, что в одном литре жидкости содержится 16 грамм солей.
Средняя соленость морских вод колеблется от 7 PSU для Балтийского моря до 40 PSU для Красного моря. Мертвое море стоит особняком, так как его соленость зашкаливает и составляет в среднем 265 PSU. Благодаря высокому содержанию солей воды Мертвого моря характеризуются плотностью на уровне 1,3 кг/м³.
Плотность
В целом литр морской воды содержит 2 столовые ложки солей. Благодаря этому плотность такой жидкости всегда больше пресной и в среднем составляет 1,025 грамм на кубический сантиметр. На плотность воды влияет не только состав, но и температура. При охлаждении морская вода сжимается, и ее плотность увеличивается.
Изменчивая плотность воды оказывает большое влияние не только на подводную жизнь, но и на морские перевозки. При переходе кораблей из океанических вод в пресные реки или переходе из тропических вод в холодные воды Атлантики, осадка судна может изменяться до 30 см, что является большой проблемой для судов, заходящих в порт. На современных грузовых судах на корпусе выполняются отметки осадки судна, которая зависит от температуры и солености воды. При прочих равных такие отметки позволяют легко определить, насколько изменилась плотность морской воды.
Пресная вода
В отличие от морской воды, пресная в своем составе практически не имеет примесей, и содержание солей в такой жидкости не превышает 0,1%. Пресная вода занимает всего 3% от общего объема воды на планете и содержится в ледниках, айсбергах, реках, подземных водах, пресных озерах и даже облаках. В целом подавляющая часть пресной воды существует на Земле в виде льда.
Интересно, что пресные айсберги курсируют по соленому океану, и возникает вопрос, как они туда попадают? Все дело в том, что морская вода испаряется, при этом теряя все соли и преснея, и скапливается в виде облаков. После этого пресная вода выпадает в виде осадков, а снег уплотняется под собственным весом и образует ледник. Айсберги — не что иное, как отколовшиеся куски ледника. Более интересно то, что когда морская вода замерзает, а это происходит при температуре минус 2 градуса, то в ней образуются тонкие ледяные кристаллы, не содержащие соль. Если выбрать эти кристаллы из океанской воды и растопить, то можно получить чистую пресную воду.
Плотность пресной воды
Плотность пресной воды зависит только от температуры. При нуле градусов по Цельсию плотность пресного льда составляет 999,8000 кг/м3, а при 100 градусов плотность пара снижается до 958,4000 кг/м3. Это табличные значения, полученные в идеальных условиях. Для определения плотности речных или озерных вод, ученые используют стандарты IPTS-68 и ITS-90. Шкала температур ITS-90 пришла на смену IPTS-68 в 1990 году в связи с пересчетом ключевых точек замерзания пресных вод. Плотность пресной воды по разным стандартам легко выражается одна через другую по формуле:
Разница небольшая, но именно ITS-90 используется в современных гидрологических расчетах.
Калькулятор плотности воды
Наша программа позволяет определить плотность пресной воды в зависимости от ее температуры тремя способами:
- найти табличное значение;
- рассчитать по формуле, использующей стандарт IPTS-68;
- вычислить по формуле ITS-90.
Температуру в калькуляторе вы можете задать в Кельвинах, Цельсиях или градусах Фаренгейта.
Плотность соленой воды зависит и от температуры, и от ее солености, которая в нашем калькуляторе указывается в PSU (Practical Salinity Units), что идентично понятию промилле. Рассмотрим пример.
Вычисление плотности при помощи калькулятора
Давайте вычислим плотность питьевой дистиллированной воды при комнатной температуре 20 градусов по шкале Цельсия. Для определения плотности требуется выбрать шкалу температуры и метод вычисления. Используем все три метода и получим:
- табличное значение — 998,2000 кг/м3;
- стандарт IPTS-68 — 997,9355 кг/м3;
- стандарт ITS-90 — 997,6699 кг/м3.
Как видите, различия минимальны, но при точных расчетах неверный выбор значения может привести к ошибкам.
Теперь подсчитаем плотность воды Красного моря, соленость которого составляет 40 PSU при температуре 30 градусов Цельсия. Введите эти данные в соответствующие ячейки и вычислите результат: 1 028,5825 кг/м3.
Заключение
Плотность воды — важный параметр, который используется в химии, физике, гидрологии и мореплавании. Используйте наш калькулятор для быстрого вычисления плотности воды в зависимости от ее температуры и солености.
Источник
Таблица плотности веществ
Плотность — физическая величина, которая равна отношению массы тела к его объему:
Плотности некоторых твердых тел (при норм. атм. давл., t = 20ºC)
| Твердое тело | ρ, кг / м 3 | ρ, г / cм 3 | Твердое тело | ρ, кг / м 3 | ρ, г / cм 3 |
|---|---|---|---|---|---|
| Осмий | 22 600 | 22,6 | Мрамор | 2700 | 2,7 |
| Иридий | 22 400 | 22,4 | Стекло оконное | 2 500 | 2,5 |
| Платина | 21 500 | 21,5 | Фарфор | 2 300 | 2,3 |
| Золото | 19 300 | 19,3 | Бетон | 2 300 | 2,3 |
| Свинец | 11 300 | 11,3 | Кирпич | 1 800 | 1,8 |
| Серебро | 10 500 | 10,5 | Сахар-рафинад | 1 600 | 1,6 |
| Медь | 8 900 | 8,9 | Оргстекло | 1 200 | 1,2 |
| Латунь | 8 500 | 8,5 | Капрон | 1 100 | 1,1 |
| Сталь, железо | 7 800 | 7,8 | Полиэтилен | 920 | 0,92 |
| Олово | 7 300 | 7,3 | Парафин | 900 | 0,90 |
| Цинк | 7 100 | 7,1 | Лёд | 900 | 0,90 |
| Чугун | 7 000 | 7,0 | Дуб (сухой) | 700 | 0,70 |
| Корунд | 4 000 | 4,0 | Сосна (сухая) | 400 | 0,40 |
| Алюминий | 2 700 | 2,7 | Пробка | 240 | 0,24 |
Плотности некоторых жидкостей (при норм. атм. давл., t = 20ºC)
| Жидкость | ρ, кг / м 3 | ρ, г / cм 3 | Жидкость | ρ, кг / м 3 | ρ, г / cм 3 |
|---|---|---|---|---|---|
| Ртуть | 13 600 | 13,60 | Керосин | 800 | 0,80 |
| Серная кислота | 1 800 | 1,80 | Спирт | 800 | 0,80 |
| Мёд | 1 350 | 1,35 | Нефть | 800 | 0,80 |
| Вода морская | 1 030 | 1,03 | Ацетон | 790 | 0,79 |
| Молоко цельное | 1 030 | 1,03 | Эфир | 710 | 0,71 |
| Вода чистая | 1000 | 1,00 | Бензин | 710 | 0,71 |
| Масло подсолнечное | 930 | 0,93 | Жидкое олово (при t = 400ºC) | 6 800 | 6,80 |
| Масло машинное | 900 | 0,90 | Жидкий воздух (при t = -194ºC) | 860 | 0,86 |
Плотности некоторых газов (при норм. атм. давл., t = 20ºC)
| Газ | ρ, кг / м 3 | ρ, г / cм 3 | Газ | ρ, кг / м 3 | ρ, г / cм 3 |
|---|---|---|---|---|---|
| Хлор | 3,210 | 0,00321 | Оксид углерода (II) (угарный газ) | 1,250 | 0,00125 |
| Оксид углерода (IV) (углекислый газ) | 1,980 | 0,00198 | Природный газ | 0,800 | 0,0008 |
| Кислород | 1,430 | 0,00143 | Водяной пар (при t = 100ºC) | 0,590 | 0,00059 |
| Воздух (при 0ºC) | 1,290 | 0,00129 | Гелий | 0,180 | 0,00018 |
| Азот | 1,250 | 0,00125 | Водород | 0,090 | 0,00009 |
Источник
Насыпная плотность технической соли
Средняя насыпная плотность технической соли — 1100-1150 кг на 1 куб.м. Это характерно для соли 3-го помола с уровнем влажности до 7%. Насыпная плотность может уменьшаться и увеличиваться, исходя из влажности и фракции материала. Минимальный показатель — 800 кг на 1 куб.м, максимальный — 1300 кг на 1 куб.м.
Источник
Плотность солей. Температура плавления соли
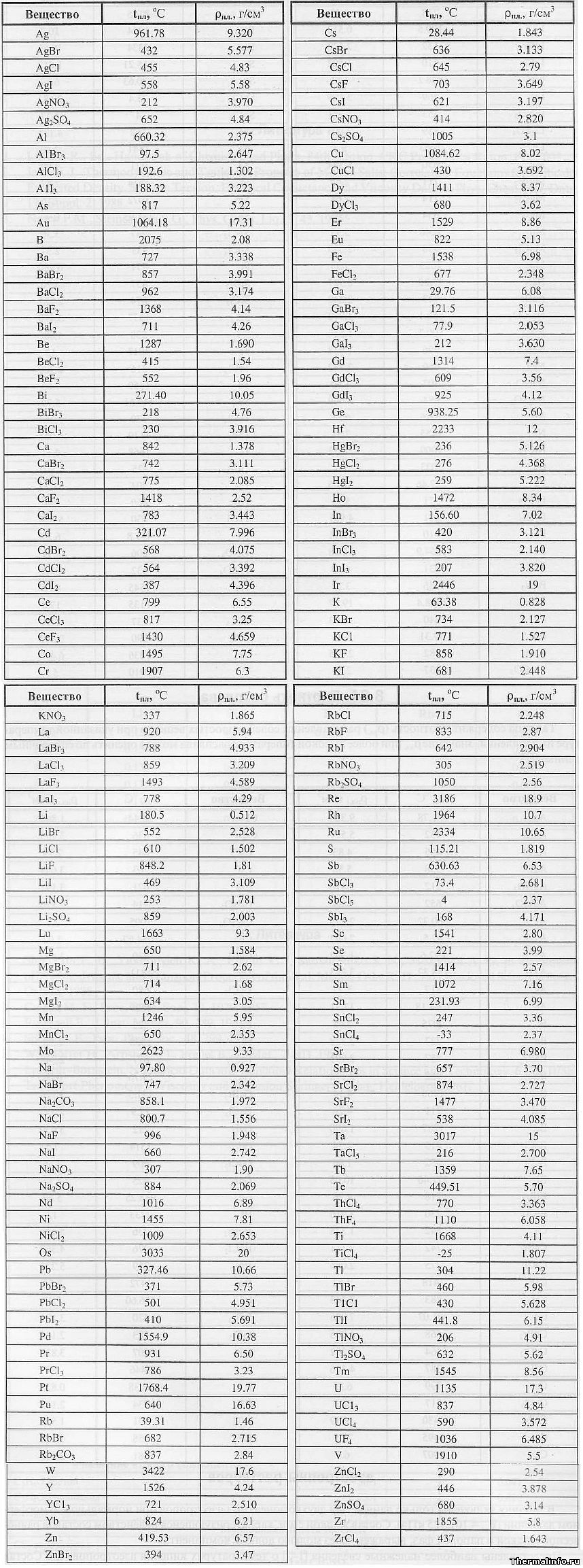
В таблице представлена плотность расплава солей (жидкой соли) и элементов, образующих эти соли, а также их температура плавления. Плотность соли дана при температуре расплава, в размерности г/см 3 .
Рассмотрены следующие соли: бромид, хлорид, йодид, нитрат, сульфат, фторид, карбонат; соли следующих металлов: серебра, алюминия, мышьяка, золота, бора, бария, бериллия, висмута, кальция, кадмия, церия, кобальта, хрома, цезия, меди, диспрозия, эрбия, европия, железа, галлия, гадолиния, германия, гафния, ртути, гольмия, индия, иридия, калия, лантана, лития, лютеция, магния, марганца, молибдена, натрия, неодима, никеля, осмия, свинца, палладия, празеодима, платины, плутония, рубидия, рения, родия, рутения, сурьмы, скандия, селена, самария, олова, стронция, тантала, тербия, теллура, тория, титана, таллия, тулия, урана, ванадия, вольфрама, иттрия, иттербия, цинка, циркония.
Следует отметить, что наибольшей плотностью обладают жидкие соли таких тяжелых металлов, как свинец и уран. Например, плотность расплавов солей йодида свинца PbI2, по данным таблицы, равна 5,691 г/см 3 , а плотность тетрафторида урана UF4 составляет величину 6,485 г/см 3 . К легким солям, с малой плотностью относятся соли алюминия, бериллия, лития, калия и циркония.
Плотность большинства солей в жидком состоянии меньше, чем в твердом. Это объясняется увеличением объема соли при нагревании — жидкая соль всегда находится при высоких температурах. Например, плотность поваренной соли NaCl в кристаллическом состоянии при комнатной температуре равна 2,17 г/см 3 , а плотность жидкого хлорида натрия (при температуре 801°С) уменьшается и становится равной 1,556 г/см 3 .
Наименьшая температура плавления соли в таблице соответствует хлориду олова SnCl4 — он плавится при температуре минус 33°С, то есть при комнатной температуре находится в жидком состоянии и на воздухе дымит из-за реакции с парами воды.
Самой тугоплавкой солью с максимальной температурой плавления, по данным таблицы, является фторид лантана LaF3 — фтористый лантан плавится при температуре 1493°С.
Источник:
Волков. А.И., Жарский. И.М. Большой химический справочник. — М: Советская школа, 2005. — 608 с.
Источник