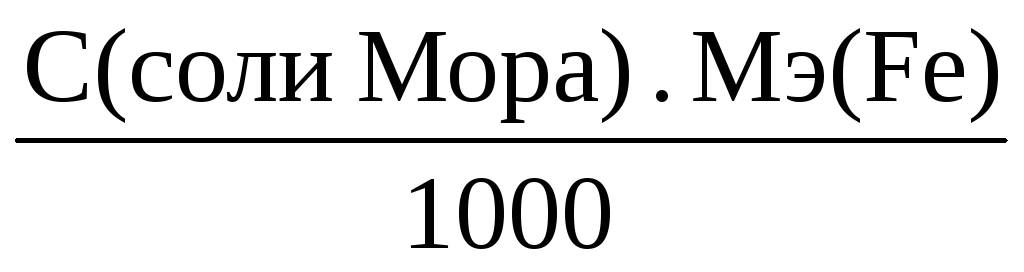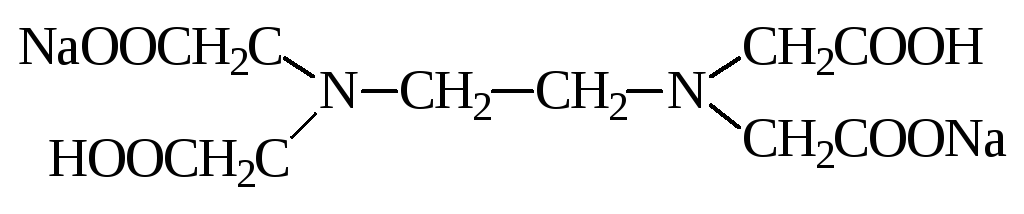Опыт 2. Определение железа (II) в растворе соли Мора
При взаимодействии соли Мора с перманганатом калия соль закиси железа (Fe 2+ ) окисляется в соли окиси (Fe 3+ ) по уравнению:
Выполнение работы. В мерную колбу емкостью 100 мл возьмите немного соли Мора добавьте дистиллированной воды до метки и хорошо перемешайте. Полученным раствором ополосните пипетку и перенесите 10мл исследуемого раствора в колбу. Добавьте цилиндром 8-10 мл 2н серной кислоты и титруйте перманганатом калия холодный раствор (нагревание способствует окислению Fe 2 + кислородом воздуха до Fe 3+ ). Титрование вести до появления бледно розовой окраски, не исчезающей в течение 1 мин. Повторите титрование не менее 3 раз, возьмите среднее из отчетов и вычислите количество граммов железа в исследуемом растворе.
Вычисление. Нормальность Fe 2 + в соли Мора вычислите по затраченным на титрование объемом растворов (нормальность KMnO4известна из предыдущей работы ). Умножив нормальность на грамм- эквивалент железа (55,85г) найдете количество железа в 1 л раствора.
Опыт 3. Определение содержания кальция в растворе.
Катион Ca 2+ не отдаёт электронов, не может быть восстановлен и не реагирует с перманганатом калия. поэтому количество его нельзя определять непосредственным титрованием раствора перманганатом. Определение выполняют косвенным методом.
Из анализируемого раствора ионы Ca 2+ осаждают действием щавелевой кислоты или оксалата натрия.
Осадок оксалата кальция отфильтровывают, промывают и обрабатывают горячей разбавленной серной кислотой. При этом в раствор переходит эквивалентное кальцию количество щавелевой кислоты:
Щавелевую кислоту титруют рабочим раствором перманганата калия:
При вычислении надо учитывать, что эквивалент H2C2O4*2H2O в данном случае равен Ѕ грамм- молекулы, а эквивалент Ca 2+ соответственно Ѕ его грамм- атома, т. е 20,04 г.
Выполнение работы.В химический стакан возьмите для анализа немного раствора соли Ca 2+ (около 0,05 г Ca 2+ ). Прибавьте к нему 5- 6 мл 1 н. раствора щавелевой кислоты и нагрейте смесь до кипения. Затем, добавив 2- 3 капли метилового оранжевого медленно нейтрализуйте жидкость аммиаком до перехода красной окраски индикатора в желтую. Содержимому стакана дайте постоять до тех пор, пока осадок оксалата кальция CaC2O4 соберется на дне. Осадок отфильтровывают через синий фильтр, промывают, затем растворяют в серной кислоте разбавляя (1:5) и освободившуюся щавелевую кислоту титруют раствором перманганата калия. Количество перманганата калия, пошедшее на окисление щавелевой кислоты, эквивалентно количеству кальция. Процесс титрования заканчивают с появлением в растворе слабо- малинового цвета, титрование повторяют 2- 3 раза.
Количество Ca 2+ в растворе вычисляют по формуле:
N KMnO4 – нормальность, V KMnO4 — объём средний израсходованного в процессе титрования, ЭCa – грамм- эквивалент Ca 2+
Иодометрия-метод количественного объемного анализа, в основе которого лежит реакция восстановления свободного йода в йод-ион или окисления йод-иона в свободный иод. Направление реакции зависит от окислительной способности вступающих в реакцию с йодом веществ: например с Na2S2O3 реакция идет слева направо, с КМп04, К2Сг2О7-справа налево. Степень окислительной способности кислородсодержащих соединений зависит от активной реакции среды (концентрации ионов); меняя ее, легко можно изменить направление процесса. Главнейшей в йодометрии реакцией является восстановление J раствором тиосульфата натрия (гипосульфита натрия- Na2S2O3). Индикатором при титровании служит обычно раствор крахмала (0,2%-ного раствора на 100 см 3 жидкости), дающего с йодом в присутствии растворимых иодидов синее окрашивание. При титровании до исчезновения синего окрашивания последнее часто вновь появляется через некоторое время. Это может зависеть 1) от медленного течения реакции восстановления йода; 2) от окислительных процессов за счет кислорода воздуха (особенно при солнечном свете); 3) от участия в реакции посторонних веществ; особенно сильно влияет азотистая кислота; присутствуя в ничтожном количестве (напр. в лабораторном воздухе). Для приготовления раствора Na2S2O3 около 25 г химически чистого препарата) растворяют в 1 л воды и устанавливают титр спустя 10-14 дней после приготовления. Раствор тиосульфата нужно хранить в темном месте и титр следует проверять раз в 2 месяца.
Децинормальный раствор иода готовится растворением 12,8-13 г иода и 25 г йодистого калия в 1 литре воды. Раствор не стоек, и титр его следует проверять; раствор надо хранить в темноте. Титр устанавливают по раствору тиосульфата. Благодаря очень большой чувствительности реакции иода с крахмалом и отчетливости изменения цвета при конце титрования. Йодометрия считается одним из лучших методов коли-чественного анализа и получила широкое применение в химии.
Лабораторная работа
Опыт 1. Приготовление рабочего раствора тиосульфата натрия и определение его концентрации по титрованному раствору перманганата калия.
Рассмотрим окислительно-восстановительные процессы в реакции тиосульфата натрия с йодом:
Так как два иона S2O3 2- Теряют два электрона (по одному на каждый ион), то грамм-эквивалент восстановителя (тиосульфата натрия) равен:
Приготовить титрованный раствор тиосульфата натрия по точной навеске нельзя вследствие того, что кристаллы тиосульфаты натрия на воздухе выветриваются, и химический состав их не всегда соответствует формуле Na2S2O3 · 5H2O. Поэтому тиосульфат натрия готовят приблизительной концентрации, растворяя навеску тиосульфата натрия в свежекипяченой и охлажденной дистиллированной воде. Раствор выдерживают 8-10 дней. Хранят раствор в бутыли из темного стекла с пробкой, снабженной хлоркальциевой трубкой. Концентрация тиосульфата натрия устанавливается с помощью окислителя с известной концентрации. В качестве таких окислителей применяют перманганат калия (в кислой среде), бихромат калия (в кислой среде) и йод.
Выполнение работы. В коническую колбу влить последовательно 20-25 мл. 2 н. серной кислоты, 15-20 мл. 10%-го раствора йода калия и точно отмеренный объем (отмерять пипеткой) титрированного раствора перманганата калия. Происходит реакция:
Накрыв колбу стеклом, смесь выдерживают 3-5 мин, поместив колбу в темное место. Затем добавить 100 мл дистиллированной воды и титровать тиосульфатом натрия:
Сначала титруют без крахмала до получения бледно-желтой окраски раствора. Затем, прилить 2-3 мл раствора крахмала и продолжать титровать до полного исчезновения окраски. Тиосульфат натрия следует приливать осторожно, перемешивая содержимое колбы после каждой прибавленной капли. Титрование повторить не менее трех раз. Из реакции видно, что перманганат калия непосредственно с тиосульфатом натрия не взаимодействует, но число затраченных грамм-эквивалентов тиосульфата равно числу грамм-эквивалентов йода, а последнее – числу грамм-эквивалентов перманганата калия. Поэтому, зная концентрацию перманганата калия и тиосульфата натрия, можно, пользуясь основным соотношением объемного анализа, рассчитать концентрацию тиосульфата натрия по формуле: VKMnO4· NKMnO4= VNa2S2O3· NNa2S2O3
Затем рассчитываем титр раствора тиосульфата натрия:
Опыт 2. Приготовление рабочего раствора йода и определение его нормальности и титра по титрованному раствору тиосульфата натрия.
Для приготовления раствора йода по точной навеске его необходимо очищать возгонкой. Но можно приготовить титрованный раствор и из йода без предварительной очистки. Готовится раствор приблизительно нужной концентрации, а затем определяют его нормальность по раствору тиосульфата натрия. Для приготовления 0,02 н. раствора йода отвешивают около 2,7 г. кристаллического йода (грамм-эквивалент йода равен 126,91 г; 126,91 · 0,02 = 2,54 г.) и растворяют его в концентрированном растворе йодистого калия (йод плохо растворим в воде). Растворение йода проводят в мерной литровой колбе, а затем разбавляют дистиллированной водой до метки.
Выполнение работы.В коническую колбу влить определенный объем 10мл (отмеренный пипеткой) приготовленного раствора йода. Разбавить приблизительно таким же объемом дистиллированной воды. Титровать рабочим раствором тиосульфата натрия до появления светло-желтого окрашивания. Добавить 2 мл раствора крахмала и продолжать титрование до полного обесцвечивания раствора. Нормальность раствора йода определить по уравнению:
Источник
Лабораторная работа 11 Определение железа (II) в растворе соли Мора
Определение содержания железа (II) в растворах является одним из важнейших применений перманганатометрии, которое осуществляют прямым методом титрования. Соль Мора (NH4)2Fe(SO4)2 6Н2О окисляется перманганатом калия в среде серной кислоты согласно уравнению:
В отличие от титрования оксалат-иона, данное определение проводят на холоде, так как при нагревании железо (II) окисляется кислородом воздуха до железа (III).
Ход определения. Исследуемый раствор соли Мора в мерной колбе доводят дистиллированной водой до метки. В колбу для титрования мерной пипеткой отбирают 10,0 мл анализируемого раствора, подкисляют 10–15 мл раствором H2SO4 с молярной концентрацией эквивалента 2 моль/л и титруют рабочим раствором перманганата калия до появления устойчивой бледно-розовой окраски. Повторяют титрование 23 раза, результаты записывают в таблицу 8 и определяют содержание железа (II) по формулам:
С(соли Мора) = (моль/л);
Т(соли Мора/Fe) = (г/мл);
m(Fe) = Т(соли Мора/Fe) . Vколбы (г).
Железо (II) окисляется до железа (III), теряя один электрон. Поэтому молярная масса эквивалента железа равна его атомной массе 55,85.
9.3. Комплексонометрическое титрование
Метод основан на реакции образования прочных комплексных соединений ионов металлов с рядом комплексообразующих органических реагентов, получивших название комплексонов. Связывание определяемого катиона в комплекс происходит тем полнее, чем прочнее образующийся комплекс. Для этого титрование комплексонами проводят при строго определенных условиях, из которых наибольшее значение имеет рН титруемого раствора.
Наибольшее значение из комплексонов имеет двунатриевая соль этилендиаминтетрауксусной кислоты ЭДТА, которую называют также комплексоном III или трилоном Б.
Комплексон III образует со многими катионами достаточно прочные и растворимые в воде внутрикомплексные соли в результате замещения атомов водорода функциональных групп органического реагента, на катион металла. Одновременно катион металла взаимодействует с атомами азота аминогруппы посредством координационной связи:
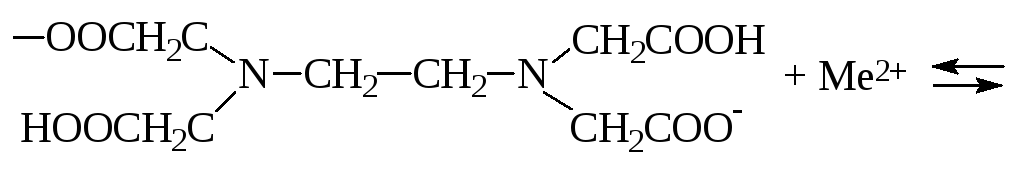
Со всеми ионами металлов (кроме одновалентных) ЭДТА реагирует в отношениях 1:1. В умеренно кислых растворах эти реакции могут быть записаны в следующем виде:
Таким образом, молярная масса эквивалента любого металла будет равна 1/2 его атомной массы. Поскольку степень комплексообразования зависит от рН, титрование раствором ЭДТА проводят при постоянном рН, которое достигается добавлением буферного раствора.
В качестве индикаторов применяют интенсивно окрашенные красители (металлоиндикаторы), образующие с титруемыми ионами металлов комплексы различной окраски. Чаще всего в практике используют эриохром черный Т, мурексид, ксиленоловый оранжевый и др.
В зависимости от рН раствора эриохром черный Т существует в трех окрашенных формах:
Источник
Определение соли мора титрование
- Главная
- Химия
- Окислительно-восстановительное титрование
- Определение железа в растворе соли Мора
Определение железа в растворе соли Мора
Опыт 2. Определение железа (II) в растворе соли Мора.
Принцип метода. Титрование железа (II) основано на реакции:
5Fe2+ + MnO4-+ 8H+ ® 5Fe3+ + Mn2+ + 4H2O.
Если железо (II) входит в состав соли Мора (NH4)2SO4·FeSO4·6H2O, то идёт следующая реакция:
2KMnO4 + 10(NH4)2SO4·FeSO4 + 8H2SO4 ® 2MnSO4 + 5Fe2(SO4)3 + K2SO4 +
10 5 Fe2+ — e — ® Fe3 + 2 1 MnO4- + 8H+ + 5e — ® Mn2+ + 4H2O
Реагенты и оборудование: стандартизованный 0,05 н раствор перманганата калия; раствор соли Мора; 2 н раствор серной кислоты; бюретка; стеклянная воронка; конические колбы ёмкостью 100 мл; пипетки Мора; стеклянный цилиндр ёмкостью 50 мл; мерная колба ёмкостью 100 мл.
Ход анализа. В мерную колбу ёмкостью 100 мл наливают немного раствора соли Мора, доводят объём дистиллированной водой до метки и перемешивают. Из этого раствора пипеткой Мора отбирают 10,00 мл и переносят в коническую колбу, добавляют 10 мл 2 н раствора серной кислоты. В чистую бюретку заливают раствор перманганата калия и подготавливают к титрованию. Титрование подкисленного раствора соли Мора перманганатом калия проводят на холоде (при нагревании катион железа (II) окисляется кислородом воздуха до катиона железа (III)) до появления бледно-малиновой окраски, не исчезающей при встряхивании в течение 1-2 минут. Повторяют титрование 2-3 раза.
Обработка результатов. Из сходящихся отсчётов берут средний результат титрования и вычисляют массу железа в анализируемом растворе.
.
Масса железа в 100 мл раствора соли Мора равна:
Источник