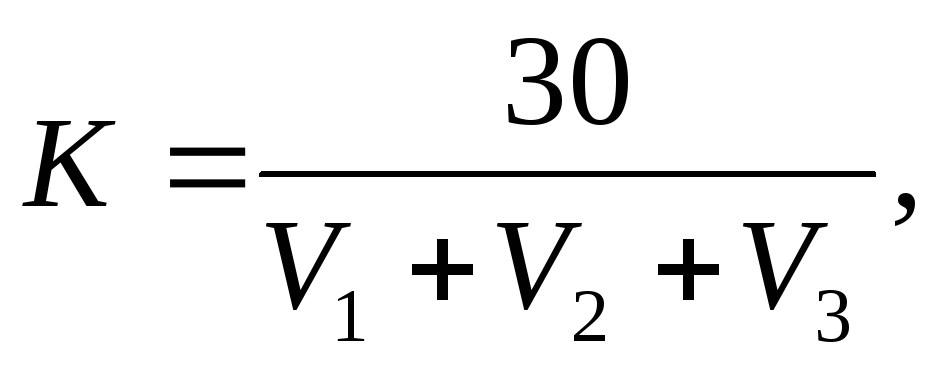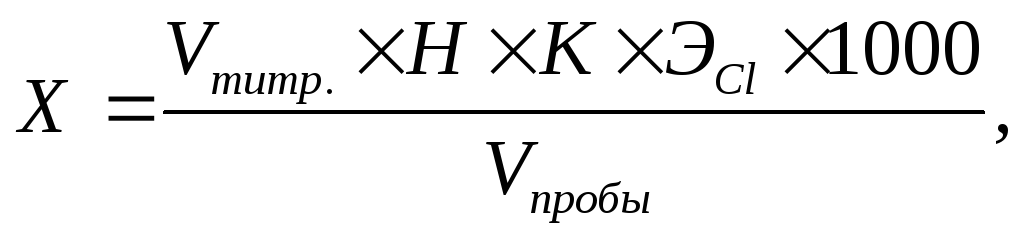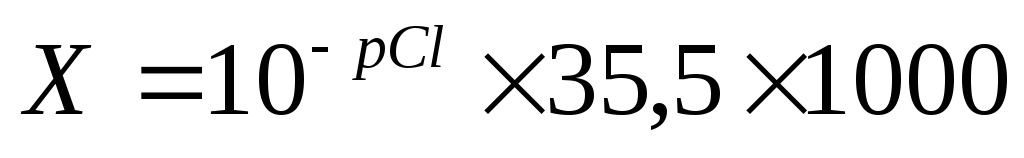- Определение хлоридов в воде
- Порядок выполнения работы
- I. Определение хлоридов в воде методом Мора
- Лабораторная работа № 20 Аргентометрическое определение хлоридов по методу Мора
- Ход определения
- Лабораторная работа № 21 Определение хлоридов с помощью ионоселективного электрода
- Ход определения.
- 5.5. Определение содержания хлора в образце по Мору
- 5.6. Приготовление стандартизированного раствора тиоцианата аммония
Определение хлоридов в воде
Оборудование: а) метод Мора: конические колбы на 200 мл; пипетки на 10 мл; цилиндры мерные на 100 мл; бюретки для титрования; дистиллированная вода; 0,01 н раствор AgNO3; 0,01 н раствор NaCl; 5%-ный раствор К2СгО4; б) приближенный метод: пробирки, пипетки, азотная кислота (1: 3), 10%-й раствор нитрата серебра
Высокая растворимость хлоридов объясняет широкое их распространение во всех природных водах. Хлориды в воде могут быть минерального и органического происхождения и встречаться в форме солей — NaCl, KC1, MgCl2, СаС12. В южных регионах повышенное содержание хлоридов в воде обычно связано с засоленностью грунтов, богатых хлористыми соединениями. Такая вода не представляет опасности в санитарном отношении. Хлориды органического происхождения образуются при разложении органических веществ, преимущественно мочи, фекалий и др.
При централизованном и нецентрализованном водоснабжении содержание хлоридов в воде до 350 мг/л. В проточных водоемах концентрация хлоридов обычно невелика (20-30 мг/л). Незагрязненные грунтовые воды в местах с несолончаковой почвой обычно содержат до 30-50 мг/л хлор-иона. В водах, фильтрующихся через солончаковую почву, в 1 л могут быть сотни и даже тысячи миллиграммов хлоридов. Вода, содержащая хлориды в концентрации более 350 мг/л, имеет солоноватый привкус. При концентрации хлоридов 500-1000 мг/л вода неблагоприятно влияет на желудочную секрецию. Содержание хлоридов является показателем загрязнения подземных и поверхностных водоисточников и сточных вод.
Определение концентрации хлоридов в воде можно провести двумя способами:
а) методом Мора. Принцип метода Мора основан на осаждении хлоридов азотнокислым серебром в присутствии хромата калия К2СrO4. При наличии в растворе хлоридов AgNO3 связывается с ними, а затем образует хромат серебра оранжево-красного цвета.
б) приближенным методом. Он основан на осаждении хлоридов азотнокислым серебром, реакция протекает по уравнению:
Порядок выполнения работы
I. Определение хлоридов в воде методом Мора
Установить титр AgNO3. Для этого в коническую колбу на 200 мл налить 10 мл раствора NaCl и 90 мл дистиллированной воды, прибавить 5 капель К2СrO4. Содержимое колбы оттитровать раствором AgNO3 до перехода лимонно-желтой окраски мутного раствора в оранжево-красную, не исчезающую в течение 15-20 с.
Рассчитать поправочный коэффициент к титру AgNO3 по результатам трех титрований.
где П — объем в мл AgNO3, использованный на каждое титрование.
При содержании хлоридов менее 250 мг/л взять 100 мл фильтрованной испытуемой воды. При большем содержании хлоридов -10-50 мл. Испытуемую воду налить в две конические колбы, довести до 100 мл дистиллированной водой, прибавить 5 капель раствора К2СгО4. Раствор в одной колбе титровать AgNO3, а вторая колба используется для контроля.
Источник
Лабораторная работа № 20 Аргентометрическое определение хлоридов по методу Мора
Сущность метода.Метод Мора основан на осаждении хлоридов азотнокислым серебром в присутствии хромата калияK2CrO4. Нитрат серебра при наличии в растворе хлоридов первоначально реагирует с ними, а лишь затем после связывания всех хлоридов образуется хромат серебра оранжево-красного цвета.
Реактивы и оборудование
Нитрат серебра, раствор 0,01 моль-экв/дм 3
Хлорид натрия, раствор 0,01 моль-экв/дм 3
Конические колбы для титрования
Ход определения
При содержании хлоридов менее 250 мг/дм 3 берут 100 см 3 фильтрованной испытуемой воды. При большем содержании хлоридов берут 10 – 50 см 3 исследуемой воды и разбавляют до 100 см 3 дистиллированной водой. В две конические колбы для титрования вносят по 100 см 3 анализируемой воды, прибавляют по 5 капель раствораK2CrO4. Раствор в одной колбе титруют 0,01 Н AgNO3 до изменения окраски раствора по сравнению с окраской во второй колбе (цветной свидетель).
Стандартизация титранта. Для стандартизации титранта в коническую колбу вносят 10 см 3 0,01 Н раствораNaCд и 90 см 3 дистиллированной воды, прибавляют 5 капельK2CrO4. Содержимое колбы титруют 0,01 Н растворомAgNO3до перехода лимонно-желтой окраски мутного раствора в оранжево-красную, не исчезающую в течение 15 – 20 сек.
Поправочный коэффициент к титруAgNO3рассчитывают по результатам трех титрований
где V1, V2, V3 – объемы AgNO3, пошедшие на каждое из трех титрований, см 3 .
Расчет. Содержание хлорид-иона Х (мг/дм 3 ) рассчитывают по формуле:
где Vтитр. – количество раствора AgNO3, пошедшее на титрование, см 3 ;
Н – концентрация титранта – нитрата серебра, моль-экв/дм 3 ;
К – поправочный коэффициент к концентрации титранта;
ЭCl – эквивалент хлорид-иона, г/моль-экв;
Vпробы – объем воды, взятой для анализа, см 3 ;
1000 – коэффициент для перехода от граммов к миллиграммам.
Лабораторная работа № 21 Определение хлоридов с помощью ионоселективного электрода
Сущность метода.Потенциометрический метод определения хлоридов основан на определении ЭДС электродной системы, состоящей из хлоридного ионоселективного электрода и вспомогательного хлоридсеребряного электрода. Он позволяет определить суммарную концентрацию хлоридов (всех его форм: иона хлора, его комплексных соединений). Метод используется для растворов с концентрацией хлоридов 0,1 – 10,0 мг/дм 3 .
Мешающие вещества. Мешают большие количества сульфидов, хлоридов, бромидов, роданидов, образующих на поверхности электрода нерастворимые соли, а также сильные восстановители и вещества, образующие комплексные соединения с серебром (например, ЭДТА).
Реактивы и оборудование
Иономер с иононоселективным хлоридным и хлоридсеребрянным электродами
Хлорид натрия, 0,1 М раствор.
Ацетатный буферный раствор
Ход определения.
Построение градуировочного графика. Из основного стандартного раствора хлорида натрия с концентрацией 0,1 М методом последовательного десятикратного разбавления готовят растворы 10 -2 М, 10 -3 М,10 -4 М, 10 -5 М, для чего 10 см 3 раствора с более высокой концентрацией наливают в колбу на 100 см 3 и доводят водой до метки. Полученные растворы имеют значения рCl= 1, 2, 3, 4, 5. В стакан вместимостью 50 см 3 вливают 20,0 см 3 рабочего стандартного раствора с рCl= 5, приливают 5 см 3 ацетатного буферного раствора, перемешивают на магнитной мешалке. Измеряют ЭДС при перемешивании раствора магнитной мешалкой. Аналогично измеряют ЭДС для других стандартных растворов. При выполнении измерений необходимо следить за тем, чтобы на поверхности мембраны хлоридного электрода не налипали пузырьки воздуха.
По результатам измерений строят градуировочный график зависимости значение ЭДС, милливольты – значение рCl.
Определение хлоридов в анализируемой воде. В стакан вместимостью 50 см 3 помещают 20 см 3 анализируемой воды (температура воды не должна отличаться от температуры стандартных растворов, по которым калибруют электрод, более чем на2 0 С, в противном случае воду следует подогреть или охладить). Затем помещают в раствор магнит от магнитной мешалки, приливают 5 см 3 буферного раствора и погружают в раствор тщательно промытые дистиллированной и анализируемой водой ионоселективный хлоридный и вспомогательный электроды. Измеряют ЭДС. По градуировочному графику находят значение рClанализируемой воды.
Расчет.Концентрация хлоридов в воде (Х) вмг/дм 3 рассчитывается по формуле:
,
где рСl– показатель концентрации хлорид-иона; найденный по графику;
35,5– молярная масса иона хлора, г/моль;
1000 – коэффициент для перехода от граммов к миллиграммам.
Источник
5.5. Определение содержания хлора в образце по Мору
Техника определения аналогична установлению нормальности раствора нитрата серебра. Содержание ионов Cl — нередко определяют в удобрениях и других сельскохозяйственных химикалиях.
Ход определения. Возьмите пробирку с образцом анализируемого вещества, содержащим то или иное количество хлорида. Взвесьте ее, перенесите содержимое пробирки в мерную колбу вместимостью 10 мл. Снова взвесьте пробирку и по разности найдите величину навески.
Растворите навеску вещества в воде, доведите объем раствора до метки, перемешайте. Отбирая пипеткой по 10,00 мл анализируемого раствора в коническую колбу, титруйте его раствором нитрата серебра в присутствии хромата калия. Из сходящихся отсчетов возьмите среднее и вычислите процентное содержание хлора в образце.
Положим, навеска вещества составляла 0,1302 г, а на титрование 10,00 мл полученного раствора пошло в среднем 4,74 мл раствора нитрата серебра. Достаточно умножить эту величину на титр раствора нитрата серебра по хлору, чтобы найти массу Cl — в 10,00 мл анализируемой жидкости: 4,74∙0,0007244 = 0,003434 г. Но весь раствор содержит хлора в десять раз больше: 0,003434∙10 = 0,03434 г. Далее вычисляют массовую долю (%) хлора в образце
Использование титра раствора нитрата серебра по хлору особенно удобно при серийных определениях иона Cl — в образцах.
5.6. Приготовление стандартизированного раствора тиоцианата аммония
Раствор NH4SCN или KSCN с точно известным титром нельзя приготовить растворением навески, так как эти соли очень гигроскопичны. Поэтому готовят раствор с приблизительной нормальной концентрацией и устанавливают ее по стандартизированному раствору нитрата серебра. Индикатором служит насыщенный раствор NH4Fe(SO4)2∙12H2O. Чтобы предупредить гидролиз соли Fe, к самому индикатору и к анализируемому раствору прибавляют перед титрованием 6 н. азотную кислоту.
Приготовление 100 мл приблизительно 0,05 н. раствора тиоцианата аммония. Молярная масса эквивалента NH4SCN равна его молярной массе, т.е. 76,12 г/моль. Поэтому 0,1л 0,05н. раствора должны содержать 76,12∙0,05∙0,1 = 03806 г NH4SCN.
Возьмите на аналитических весах навеску около 0,3-0,4 г, перенесите в колбу вместимостью 100 мл, растворите, доведите объем раствора водой до метки и перемешайте.
Стандартизация раствора тиоцианата аммония по нитрату серебра. Подготовьте бюретку для титрования раствором NH4SCN. Ополосните пипетку раствором нитрата серебра и отмерьте 10,00 мл его в коническую колбу. Добавьте 1 мл раствора NH4Fe(SO4)2 (индикатор) и 3 мл 6 н. азотной кислоты. Медленно, при непрерывном взбалтывании, приливайте из бюретки раствор NH4SCN. Титрование прекратите после появления коричнево-розовой окраски [Fe(SCN)] 2+ , не исчезающей при энергичном встряхивании.
Повторите титрование 2-3 раза, из сходящихся отсчетов возьмите среднее и вычислите нормальную концентрацию NH4SCN.
Допустим, что на титрование 10,00 мл 0,02043 н. раствора нитрата серебра пошло в среднем 4,10 мл раствора NH4SCN. Тогда
с (NH4SCN) ∙ 4,10 = 0,02043∙10,00; с (NH4SCN) = 0,02043∙10,00/4,10 = 0,04982.
Источник