Фонтановая процедура — Fontan procedure
| Процедура Фонтана или Фонтана – Крейцера | |
|---|---|
 |
Процедура Фонтана или процедура Фонтана – Крейцера — это паллиативная хирургическая процедура, используемая у детей с моножелудочковым сердцем. Он включает отведение венозной крови из нижней полой вены (НПВ) и верхней полой вены (ВПВ) в легочные артерии без прохождения через морфологический правый желудочек ; то есть системное и легочное кровообращение размещаются последовательно с функциональным единичным желудочком. Первоначально процедура была выполнена в 1968 году Фрэнсисом Фонтаном и Юджином Боде из Бордо, Франция, опубликована в 1971 году, одновременно описана в 1971 году Гильермо Кройцером из Буэнос-Айреса, Аргентина, и наконец опубликована в 1973 году.
Содержание
Показания
Процедура Фонтана используется у педиатрических пациентов, у которых имеется только один функциональный желудочек, либо из-за отсутствия сердечного клапана (например, трехстворчатая или митральная атрезия ), либо из-за нарушения перекачивающей способности сердца (например, синдром гипоплазии левого сердца или гипоплазия правого сердца). сердечного синдрома ) или сложного врожденного порока сердца, при котором восстановление двух желудочков невозможно или нецелесообразно. Единственный желудочек выполняет почти вдвое больше ожидаемого объема работы, потому что он должен перекачивать кровь для тела и легких. Пациенты обычно поступают как новорожденные с цианозом или застойной сердечной недостаточностью. Завершение фонтана обычно выполняется в возрасте 2–5 лет, но также выполняется до 2 лет.
Противопоказания
После завершения Фонтана кровь должна течь через легкие, не перекачиваясь сердцем. Поэтому дети с высоким сопротивлением легочных сосудов могут не переносить процедуру Фонтана. Часто перед операцией проводят катетеризацию сердца, чтобы проверить сопротивление. Это также причина того, что процедуру Фонтана нельзя проводить сразу после рождения; сопротивление легочных сосудов высокое внутриутробно, и для его снижения требуются месяцы. Процедура Фонтана также противопоказана пациентам с гипоплазией легочной артерии, пациентам с дисфункцией левого желудочка и значительной митральной недостаточностью.
Существует четыре варианта процедуры Фонтана:
- Вентрикуляризация правого предсердия (оригинальная методика Фонтана)
- Атриопульмональное соединение (оригинальная методика Крейцера)
- Внутрисердечное полное кавопульмональное соединение (боковой туннель) (описано Марком Де Левалем и Альдо Кастаньедой отдельно)
- Экстракардиальная полная кавопульмональная связь (описана Карло Марселети)
Подход
Ремонт фонтана обычно проводится в два этапа.
Первый этап, также называемый двунаправленной процедурой Гленна или Хеми-Фонтаном (см. Также процедуру Кавасима ), включает перенаправление бедной кислородом крови из верхней части тела в легкие. То есть легочные артерии отключены от существующего кровоснабжения (например, шунт, созданный во время процедуры Норвуда , открытый артериальный проток и т. Д.). Верхней полой вены (ВПВ), которая несет кровь возвращается из верхней части тела, отсоединен от сердца , и вместо этого переадресованы в легочной артерии. Нижней полой вены (НПВ), которая несет кровь возвращается из нижней части тела, продолжает подключаться к сердцу.
Второй этап, также называемый завершением по Фонтану Крейцеру , включает перенаправление крови из НПВ в легкие. В этот момент бедная кислородом кровь из верхней и нижней части тела течет через легкие без перекачивания (управляемая только давлением, которое создается в венах). Это устраняет гипоксию и оставляет единственный желудочек, отвечающий только за кровоснабжение организма.
Послеоперационные осложнения
В краткосрочной перспективе у детей могут возникнуть проблемы с плевральным выпотом ( скопление жидкости вокруг легких). Это может потребовать более длительного пребывания в больнице для дренирования с помощью дренажной трубки . Чтобы избежать этого риска, некоторые хирурги делают отверстие из венозного кровотока в предсердие. Когда давление в венах высокое, часть бедной кислородом крови может вытечь через фенестрацию, чтобы снизить давление. Однако это приводит к гипоксии , поэтому со временем может потребоваться закрытие окна интервенционным кардиологом .
В обзоре 2016 года д-р Джек Рычик, руководитель программы по выживанию после одного желудочка в Детской больнице Филадельфии, резюмировал долгосрочные последствия кровообращения Фонтана как «вялотекущее и прогрессирующее состояние сердечной недостаточности» с предсказуемыми долгосрочными последствиями для нескольких системы органов. Предполагается, что хроническая венозная гипертензия и снижение сердечного выброса лежат в основе лимфатических осложнений, таких как хилоторакс , энтеропатия с потерей белка и пластический бронхит, которые могут возникнуть как в ближайшем послеоперационном периоде, так и в среднесрочной перспективе. Были исследованы новые интервенционные и хирургические стратегии для облегчения лимфатических осложнений, связанных с кровообращением по фонтану. Опасения по поводу повреждения печени возникли совсем недавно, поскольку кровообращение по Фонтану вызывает застой и лимфедему в этом органе, что приводит к прогрессирующему фиброзу печени . Протоколы скрининга и стандарты лечения появляются в свете этих открытий.
Процедура Фонтана является паллиативной, а не лечебной, но почти в 70% случаев она может привести к нормальному или почти нормальному росту, развитию, толерантности к физической нагрузке и хорошему качеству жизни. Однако в 20–30% случаев пациентам в конечном итоге потребуется трансплантация сердца, и, учитывая долгосрочные последствия хронической венозной гипертензии и коварного повреждения органов, избавление от болезней в долгосрочной перспективе маловероятно.
История
Процедура Фонтана была впервые описана в 1971 году доктором Фрэнсисом Фонтаном (1929–2018) из Бордо, Франция. До этого хирургическое лечение атрезии трикуспидального клапана заключалось в создании шунта между системной артерией и легочной артерией ( шунт Блэлока-Тауссига ) или верхней полой веной и легочной артерией (шунт Гленна). Эти процедуры были связаны с высоким уровнем смертности, обычно приводящей к смерти в возрасте до одного года. Пытаясь исправить это, Фонтан в период с 1964 по 1966 год занимался исследованиями, пытаясь полностью перенаправить поток из верхней и нижней полой вены в легочную артерию. Его первые попытки на собаках были безуспешными, и все экспериментальные животные умерли в течение нескольких часов; однако, несмотря на эти неудачи, он успешно выполнил эту операцию у молодой женщины с атрезией трикуспидального клапана в 1968 году вместе с доктором Юджином Боде. Операция была завершена второму пациенту в 1970 году, а после третьего случая эта серия была опубликована в международном журнале Thorax в 1971 году. Доктор Гильермо Крейцер из Буэнос-Айреса, Аргентина (род. 1934), не зная об опыте Фонтана, провел аналогичная процедура была проведена в июле 1971 г. без установки клапана во впускной канал нижней полой вены и введения концепции «фенестрации», оставляющей небольшой дефект межпредсердной перегородки, служащий откидным клапаном для кровообращения.
Источник
Операция фонтана что это
Следующие 4 раздела посвящены порокам, при которых обычно выполняют операцию Fontan. К ним относятся атрезия трехстворчатого клапана, синдром гипоплазии левых отделов сердца, двуприточный желудочек и изо-меризм.
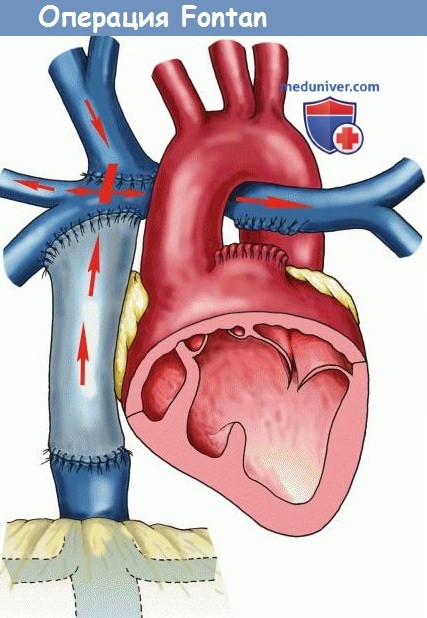
Операция Fontan — обобщающий термин, характеризующий паллиативную хирургическую процедуру, в результате которой венозная кровь из системной циркуляции направляется непосредственно в ЛА, не попадая в соответствующий (связанный с ЛА) желудочек. Эту операцию выполняют пациентам, имеющим функционально единый желудочек, или в тех случаях, когда проведение внутрисердечной коррекции невозможно даже при наличии двух желудочков нормальных размеров.
Несмотря на то что операция Fontan, несомненно, несовершенна, с ее помощью удается восстановить последовательность легочно-системной циркуляции и устранить хроническую перегрузку объемом системного желудочка, который обеспечивал параллельную легочную и системную циркуляцию. Сначала операция Fontan заключалась в простом атриопульмональном соединении, при котором ПП или его ушко анастомозировали с ЛА. Поскольку это приводило к дилатации предсердия, нарушениям ритма и тромбозам в отдаленном периоде, от данной техники операции отказались в пользу более совершенной.
В начале 1990-х гг. был предложен тотальный кавопульмональный анастомоз. Он представляет собой прямой верхний кавопульмональный анастомоз по типу «конец в бок» (двунаправленный шунт Glenn) в сочетании с внутрипредсердным соединением НПВ с нижней поверхностью сливающихся между собой ЛА.
В последнее время НПВ соединяют с ЛА посредством экстракардиального кондуита, что полностью исключает ПП из циркуляции. В дальнейшем остается оценить, приведет ли данная модификация к уменьшению поздней заболеваемости. Все пациенты после подобного вмешательства нуждаются в регулярном тщательном обследовании в специализированных центрах.
Как было отмечено ранее, неоднозначность природы циркуляции после операции Fontan, а также частая несостоятельность циркуляции обусловливают необходимость регулярного наблюдения больных в центрах, специализирующихся на лечении пациентов с ВПС, а появление новых симптомов должно быть основанием для немедленного повторного обследования в подобном центре.
С момента первой операции Fontan по поводу атрезии трехстворчатого клапана в 1971 г. данное вмешательство стало общепринятым паллиативным методом хирургической коррекции при невозможности восстановления бивентрикулярной циркуляции. В основе этой операции лежит переведение системного венозного возврата непосредственно в ЛА, минуя соответствующий «легочный» (связанный с ЛА) желудочек.
Со временем были предложены и выполнены многочисленные модификации метода: прямое атриопульмональное соединение, тотальное кавопульмональное соединение и экстракардиальный кондуит. В ряде случаев во время хирургического вмешательства у пациентов высокого риска выполняют фенестрирование (диаметром 5 мм) пути кровотока по Fontan в предсердие, обеспечивающее шунтирование справа налево и декомпрессию после операции.
Патофизиология операции Fontan. Неизбежными следствиями операции Fontan являются повышение центрального венозного давления и уменьшение СВ при физической нагрузке (но иногда в покое). Причинами серьезных, клинически выраженных нарушений также могут быть небольшое ухудшение функции желудочка (особенно диастолической), снижение эффективности функционирования (повышенное ЛСС, обструкция, тромбоз) и нарушения ритма.
Хотя больных, перенесших операцию Fontan, справедливо считают пациентами с ХСН (после вмешательства давление в ПП должно быть высоким), выраженная систолическая дисфункция редко бывает ее причиной. В действительности даже незначительное повышение диастолического давления в желудочке может быть значительно опаснее. Следовательно, лечение таких больных традиционными лекарственными средствами, применяемыми при СН, нужно считать некорректным. В одном из рандомизированных слепых плацебо-контролируемых исследований было продемонстрировано, что применение ИАПФ не привело к улучшению функционального статуса, а некоторые показатели даже ухудшились.
Более «ламинарная» циркуляция по Fontan (тотальный кавопульмональный анастомоз, экстракардиальный кондуит), в которой ПП исключено из циркуляции, имеет лучшие динамические свойства кровотока и более совершенные функциональные характеристики. Все физические препятствия в области хирургических анастомозов, дистальных ЛА или легочных вен (часто в результате сдавления дилатированным ПП) снижают эффективность циркуляции. Подобным образом отрицательный эффект приводит к повышенному ЛСС. Это связано с тем, что ЛСС — единственный значимый фактор, ухудшающий венозный возврат и повышающий венозное давление.
О состоянии ЛСС в отдаленные сроки после операции известно относительно немного, однако в последнее время у значительного числа больных были выявлены подъем ЛСС и способность организма реагировать на ингаляцию оксида азота, что свидетельствует о легочной эндотелиальной дисфункции.
Клиника операции Fontan. У большинства больных (90%) через 5 лет после операции Fontan наблюдается СН I-II ФК. Как правило, с течением времени идет прогрессирующее ухудшение функционального статуса. Часто возникают наджелудочковые аритмии — предсердная тахикардия, ТП и ФП. В отсутствие других осложнений при физикальном осмотре выявляют повышенное, обычно непульсирующее ЯВД (на 10 см выше угла грудины, создает необходимое гидростатическое давление для прохождения СВ через легочную циркуляцию), нормально расположенную верхушку, сохранный I тон (S1), единый II тон (S2) (ЛА перевязана).
Шумы, как правило, не выявляются, их наличие свидетельствует о недостаточности системного АВ-клапана или субаортальном стенозе. Генерализованный отечный синдром и асцит могут быть признаками белок-теряющей энтеропатии.
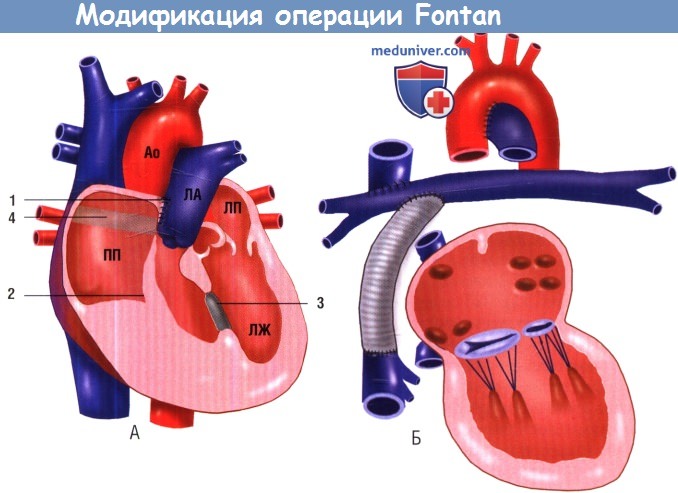
(А) Прямое атриопульмональное соединение (1) при атрезии трехстворчатого клапана (2); ушитый ДМЖП (3); ДМПП, закрытый заплатой (4).
(Б) Дакроновый экстракардиальный кондуит, соединяющий НПВ с нижней поверхностью правой легочной артерии в обход правого предсердия (ПП).
ВПВ анастомозирована с верхней поверхностью правой легочной артерии.
Ао — аорта; ЛА — легочная артерия; ЛЖ — левый желудочек; ЛП — левое предсердие.
Источник
Атрезия трехстворчатого клапана. Принцип операции Фонтена
Слово означает полное отсутствие нормального сообщения между сердечными камерами или между ними и отходящими от них магистральными сосудами, а иногда — и отсутствие отделов самих сосудов. Термин атрезия применяется к трехстворчатому, митральному, аортальному и легочному клапанным отверстиям, к аорте и легочной артерии.
Другой термин — — означает, что сообщение есть, но оно уменьшено в размерах в сравнении с нормальным. Говорят о гипоплазии трехстворчатого или митрального клапанов, отделов аорты, легочной артерии, но так же и о размерах полости одного из желудочков ().
Атрезия трехстворчатого клапана
В нормально развитом сердце соединяет правое предсердие с правым желудочком. При атрезии этот клапан не развился и на его месте имеется плотная мембрана, через которую поток крови пройти никак не может. Поскольку этот участок закрыт, то у плода не развился и тоже отсутствует весь приточный отдел правого желудочка, т.е. первый из двух конусов, образующих желудочек. Таким образом, измененным оказывается не только клапан, но и весь правый желудочек — у него отсутствует половина.
Однако, и плод, и родившийся ребенок могут с этим жить, во всяком случае, какое-то время. Шунтирование крови и ее смешивание в сердце происходит через дефекты в перегородках.
Из полых вен кровь попадает в нормальное правое предсердие. Но вход в желудочек — закрыт. Остается один путь: сквозь дефект межпредсердной перегородки — в левое предсердие. Затем через нормально развитый митральный клапан кровь поступает в левый желудочек. А вот здесь открыто два пути. Один — в аорту, другой — через дефект межжелудочковой перегородки — в оставшуюся часть правого желудочка (второй из конусов, который нормально развит) и отсюда — в легочную артерию и легкие.
Потоки крови в левом желудочке смешиваются — венозная кровь из полых вен, достигшая желудочка таким сложным путем, смешивается с артериальной кровью, пришедшей из вен легких.
Путь дальнейшего ее «распределения» зависит от того, куда легче идти основному потоку: в аорту или через дефект межжелудочковой перегородки — в легочную артерию и легкие. Кровь так и разделяется на два рукава, и разница в объеме двух потоков зависит от разницы сопротивления сосудов тела (т.е. большого круга кровообращения) и сопротивления, создаваемого дефектом перегородки.
В большинстве случаев существенно больший объем крови проходит в аорту и меньший — в легкие. Во-первых, значительная часть крови остается недонасыщенной, и у ребенка будет цианоз. Степень этого цианоза, однако, не столь выражена, как при полной транспозиции магистральных сосудов — ведь в желудочке все-таки происходит смешение артериальной и венозной крови. А, во-вторых, левый желудочек работает на оба круга, т.к. правого почти нет. Нагрузка, которая выпала на его долю — тяжелая, и очень она может быстро вызвать недостаточность кровообращения в большом круге — одышку, увеличение печени, отеки и т.д.
В сущности, и качество, и продолжительность жизни таких детей зависит от величины кровотока в легких, т.е. определяется размером дефектов в межжелудочковой и межпредсердной перегородках — этих, в данном случае, естественных шунтов «во спасение».
Со временем, по мере роста ребенка (и сердца) положение ухудшается, т.к. в легкие идет все меньше крови. Нарастает цианоз и около 90% детей не доживут до своего первого дня рождения, если им не оказать хирургическую помощь.
Оставшиеся 10% имеют достаточно большой дефект в перегородке, и кровоток в легкие у них нормальный, а иногда даже и усиленный. Они чувствуют себя неплохо, относительно нормально развиваются и почти не синюшные. Такие дети могут прожить более 10-15 лет, но у них постепенно будут развиваться признаки сердечной недостаточности и нарастать цианоз со всеми его осложнениями и последствиями.
Что же может быть сделано и — когда?
В лечении атрезии трехстворчатого клапана хирургия, особенно за последние два десятилетия, добилась значительных успехов и тактика лечения, выбор операции и времени ее проведения сегодня разработаны достаточно, чтобы добиться убедительных хороших результатов. Но нужно понимать, что, если у сердца изначально не было одного из четырех клапанов и большого участка одного из желудочков, то их сделать заново нельзя. Таких методов пока нет.
Поэтому весь процесс лечения сведется к созданию иных, более оптимальных путей для кровотока. Другими словами, лечение будет облегчающим, «паллиативным», и его нельзя выполнить в один раз, а надо постепенно готовить и сердце, и легкие к новым, более нормальным условиям кровотока, чем те, в которых они оказались при рождении.
Детям с выраженным цианозом в течение первых месяцев надо сделать операцию наложения анастомоза между большим и малым кругами кровообращения, как это описано для тетрады Фалло. Эта операция значительно улучшит их состояние на первых порах. Они начнут развиваться, будут выглядеть и вести себя соответственно возрасту, пройдет синюшность.
Но это — только первый, «жизнеспасающий» этап. Если больше ничего не делать, ребенок скоро снова станет очень больным и, чем хуже будет его состояние, тем более рискованными будут последующие этапы лечения.
Между первым и вторым годом жизни становится возможным выполнение второго этапа, а именно, снятие первого анастомоза и создание другого пути для венозной крови в легкие — прямое соединение верхней полой вены с легочной артерией, в обход правой половины сердца. Почему этого не делают сразу? Дело в том, что в первые месяцы жизни сопротивление сосудистого русла легких может оказаться слишком высоким. Подумайте, ведь давление в венах очень низкое — 5-7 мм ртутного столба, а мы хотим, чтобы оно было достаточным, чтобы без сердечного «насоса» кровь пассивно текла в легочную артерию. Для этого между венами и сосудами легких должна быть разница в сопротивлении и давлении, иначе кровь в легкие просто не потечет.
Бывают ситуации, и их довольно много, когда мы выполняем эту операцию — двунаправленный кавапульмональный анастомоз на первом году жизни, без ранее выполненного системно-легочного анастомоза. Данное клиническое решение принимает Ваш кардиолог и кардиохирург, вырабатывая таким образом наилучшую тактику лечения Вашего ребенка.
Мы останавливаемся на этом столь подробно, т.к. сам принцип так называемого применяется сегодня широко и при других пороках, когда сердце изменено настолько, что порок невозможно исправить хирургически. Так вот на этом, втором этапе, верхняя полая вена соединяется с легочной артерией таким образом, что кровь из нее поступает в оба легких. Иными словами, кровь от верхней половины тела уже идет туда, куда надо. Но пока — только от половины.
Дети обычно хорошо переносят операцию. Эта операция не только улучшит состояние ребенка, но и подготовит сердце и сосуды легких к третьей, заключительной стадии в процессе лечения — соединения нижней полой вены с легочной артерией.
Наилучшим моментом для выполнения третьей операции будет возраст 4-5 лет, хотя иногда ее делают и раньше этого срока.
Эта операция делается с искусственным кровообращением и заключается во вшивании большой заплаты или протеза в нижнюю полую вену одним концом и в легочную артерию — другим. Таким образом, теперь вся венозная кровь от всего организма идет в легкие, а окисленная в полном объеме — в левые отделы сердца, т.е. в его теперь единственный желудочек.
Эту операцию называют операцией Фонтена — по имени французского хирурга, который ее предложил.
Сегодня ее применяют не только при , но и при многих сложных врожденных пороках, когда хирургическое создание двух равноценных желудочков невозможно. Эта операция произвела революцию в лечении пороков, которые совсем недавно считались неоперабельными . Больным с такими пороками просто отказывали даже в самых лучших кардиоцентрах. Сегодня все изменилось, и благодаря операции Фонтена можно помочь и уже помогли тысячам больных. Сам принцип такого подхода — принцип Фонтена — однако, всего лишь паллиация, пусть и хорошо функционирующая. Операция Фонтена, т.е. заключительный этап хирургического лечения нельзя назвать «радикальной коррекцией» (как, например, при закрытии дефекта межпредсердной перегородки), к ней больше подходит название «постоянной паллиации», т.е. это не исправление порока, а последняя возможность максимальной в данном случае нормализации кровообращения. Человек живет без правого желудочка, а кровь пассивно течет в легкие из венозной системы. Здоров ли этот человек? Может ли он переносить те физические и психологические нагрузки, которые ожидают его в жизни? О том, что сегодня известно об этом, мы поговорим немного ниже, а сейчас вернемся к .
Как ни парадоксально это выглядит, но, чем тяжелее состояние ребенка с этим пороком изначально, тем яснее путь его лечения. Но каждый ребенок — индивидуален, и можно столкнуться с различными вариантами и сочетаниями внутрисердечных нарушений: слишком маленьким дефектом между предсердиями, слишком большим межжелудочковым сообщением, врожденным сужением легочной артерии и ее ветвей и т.д.
В каждом случае надо выбрать наиболее рациональный и безопасный способ помощи. Иногда следует вначале расширить межпредсердный дефект в рентгенохирургическом кабинете, иногда — наложить манжетку на легочный ствол, чтобы уменьшить легочный кровоток и предупредить развитие других осложнений. Сегодня все эти методы хорошо известны, но тактика лечения и последовательность — индивидуальны. Главное, чтобы ребенок сразу попал в специализированное учреждение, где есть соответствующий опыт.
Сможет ли ребенок долго и нормально жить, не имея одной из частей сердца — правого желудочка? Оказывается, сможет, и долго, и совсем неплохо. Сегодняшняя статистика говорит о том, что подавляющее большинство больных, живущих с «фонтеновским кровообращением», относятся к так называемому функциональному классу I-II степени, т.е. практически здоровы. Примерно четверти из них, оперированных 10 и более лет назад, потребовались повторные операции по замене ранее вшитых протезов, но сегодня по мере совершенствования техники операции, можно надеяться, что число таких случаев значительно уменьшится.
Главным осложнением в отдаленные сроки после операции является так называемая , выражающаяся в отеках, скоплении жидкости в полостях, потере белка. Оно поддается консервативному лечению. Так что будем оптимистами.
Понятно, что ребенок должен постоянно (минимум раз в полгода) наблюдаться у детского кардиолога, даже если нет видимых осложнений. Ребенок – не инвалид ни в коем случае, но наблюдать его должен квалифицированный и опытный врач.
В любом случае, вашему ребенку со сложнейшим ВПС было сделано все, что может предложить современная медицина, и это — такая же победа врачей, как и ваша.
Источник

