Морские льды в Арктике соленые или пресные?
У писателя Виктора Конецкого есть книга «Соленый лед». Это образное выражение или лед в Арктике в самом деле соленый? А если пресный, то как он получается из соленой воды?
Любой лёд и снег обычно только пресные (не соленые). Когда вода замерзает, вся соль из льда и снега вытесняется. Происходит холодная дистилляция, то есть превращение соленой морской воды в пресный лед. Но при многократном замерзании во льду может остаться соли несколько промиллей (это несколько миллионных долей), так что и такой морской лед относительно пресный. Воду при его таянии можно пить, на вкус соль не заметите, её очень мало. Поэтому полярники не пьют воду из Северного ледовитого океана, а делают запасы несоленой воды или растапливают лед или снег. Попробуйте дома заморозить соленую воду в морозильнике холодильника. Получите не соленый лед. Растопите его и можно пить не соленую воду. Итак, лед в Арктике (и не только в Арктике) не соленый!
Морские льды и снега в Арктике представляют из себя колоссальные запасы замерзшей пресной воды. Это ведь осадки — снег. А снег это пресная, почти дистиллированная вода. Соленая вода не замерзает, льды не могут быть солеными.
Вода, замерзая, образует лед.
При этом в процессе замерзания лед образуется из пресной воды, а запас соли из нее вытесняется в морскую воду, которая попадает в прослойки между пресным льдом.
Получается такой «слоеный» пирог — слой пресного льда и тонкая прослойка воды повышенной солености, которая ввиду повышенного содержания соли имеет более низкую температуру замерзания.
В процессе замерзания прослойка соленой воды может полностью вытесниться из-под льда (это обычно и происходит при длительном процессе) — тогда лед будет пресный и его можно использовать в пищу и для питья.
Если же замерзание происходит быстро или лед относительно молодой — соленая вода могла и не выйти из прослоек между льдом. Тогда лед имеет соленый вкус — это по сути конгломерат пресного льда и густого рассола.
В среднем же соленость льда из морской воды в 4 раза ниже солености морской воды (3-8 промилле), а общие пределы солености варьируются от 2 до 20 промилле.
Источник
4.11. Как правильно есть морской лед
Живущие у моря жители Севера знают, что свежий, только что замерзший лед есть или растапливать нельзя: он слишком соленый. Но старый, многолетний лед для этих целей подходит. Они также знают, что можно улучшить вкус льда, если недавно замерзшую льдину вытащить на берег, желательно весной или летом, когда тепло. Почему лед становится менее соленым при теплой погоде, когда испарение уменьшает количество воды в льдине, концентрация соли увеличивается и, казалось бы, лед должен был бы стать более соленым?
ОТВЕТ • Когда морская вода замерзает, соль (и другие примеси) не встраиваются в структуру кристалла льда, а образуют вкрапления, которые называют ячейками рассола. Ячейки рассола медленно мигрируют в слое льда, перемещаясь вниз, и поэтому соляной раствор постепенно выходит из льдины. Если температура льда повышается, например когда льдину вытаскивают и оставляют лежать на берегу на солнце, ячейки рассола перемещаются быстрее и скорость опреснения увеличивается.
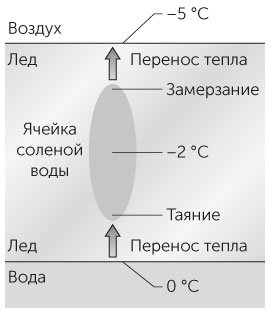
На рис. 4.2 показана ячейка рассола в слое льда. Температура льда сверху совпадает с температурой воздуха, равной –5°C; температура льда снизу равняется 0°C, то есть температуре замерзания воды, а соленая вода внутри ячейки раствора имеет температуру –2°C. Вода внутри ячейки не замерзает, поскольку соль понижает ее точку замерзания — молекулы соли влияют на способность молекул воды образовывать кристаллическую ледяную структуру. Лед в низу ячейки постепенно тает, поскольку тепло передается с низа ледяного слоя вверх. Вода в верху ячейки постепенно замерзает, поскольку тепло поднимается к поверхности слоя льда. Таким образом сама ячейка перемещается вниз. Достигнув нижней поверхности льдины, она отдает соль воде подо льдом или почве. Так постепенно лед опресняется.
Рис. 4.2 / Задача 4.11. Ячейка рассола, двигающаяся вниз через слой льда к воде.
С теплообменом между льдом и водой связан следующий удивительный результат: если кубик льда (из пресной воды), температура которого равна –1°C, поместить в очень соленую воду той же температуры, он растет, хотя температуры льда и воды равны. Чтобы объяснить, как это получается, предположим, что соль понижает точку замерзания воды до –2°C. На границе раздела между двумя состояниями воды наблюдается повышенная активность на молекулярном уровне: молекулы воды непрерывно переходят туда-сюда из льда в жидкую воду и обратно. Однако, если число молекул, ушедших из льда, равно числу молекул, перешедших в лед из воды, количество льда не меняется. В воде происходит электролитическая диссоциация молекул соли, и молекулы воды собираются вокруг получившихся ионов наподобие детей, толпящихся вокруг ларька с мороженым — этот процесс называется гидратацией. Теперь процессу перехода молекул из воды в лед мешают молекулы соли, связывающие молекулы воды. Таким образом, молекулы воды покидают кубик льда, но другие молекулы туда не поступают, и, следовательно, кубик растворяется.
Источник
Почувствуйте себя Робинзоном: как морскую воду превратить в пресную не имея ничего под рукой
Представьте себе ситуацию: судьба поменяла ваш курс и вместо райских Мальдивских островов решила внести немного огонька в вашу жизнь, отправив на необитаемый остров, где между вами и ближайшим родником километры гор. Варианта два: умереть от жажды в ожидании дождя, либо вспомнить нашу статью, где мы научим вас превращать морскую воду в пресную. Надеемся, что подобный лайфхак не пригодится, но мало ли.
Пить воду из океана — это прямой путь к обезвоживанию организма и смерти, это знают все. Хотя один смельчак все же нашелся в 1952 году. Ален Бомбар решил провести эксперимент и переплыл Атлантический океан, питаясь только океанической рыбой и запивая ее морской водой. Благодаря нему теперь известна безопасная норма потребления соленой воды — 700 миллилитров в сутки в течение семи дней. Большее количество представляет опасность для человека.
Повторять таких подвигов мы не будем, а лучше придумаем, что нам делать с морской водой, чтоб ее можно было пить без ограничений. Сразу оговоримся, что кипячение тут не поможет, а только усугубит ситуацию. Да, микроорганизмы однозначно погибнут. Но вся пресная вода уйдет вместе с паром, оставив только соль, а она приблизит вас на шаг к гибели. Но пар — уже хорошая зацепка, ведь он и есть вода, только в газообразном виде. Остается его только грамотно собрать. И для этого есть целых два способа. Правда, оба они скорее теоретические, а первый так и вовсе нам подойдет только в том случае, если мы застряли на Северном полюсе.
- Да, это замораживание. Зачерпываем морскую воду и ждем появления на поверхности кристаллов льда — они на вкус будут пресными, и такой водой вполне можно напиться.
- А вот дистилляция нам вполне подходит, главное, чтоб инструментарий был под рукой. Это перегонка воды с помощью выпаривания. А дальше два сценария развития:
Богатый Робинзон
Если повезло оказаться на острове с минимальным туристическим набором, то вам крупно повезло. Переходим к сооружению примитивного дистиллятора.
Нам понадобится:
А дальше все просто: морскую воду — в чайник, чайник — на огонь. Роем ямку в земле. В нее под наклоном зарываем стеклянную бутылку или пустой кокос так, чтобы из песка торчало только горлышко, в которое вставляется передающая пар трубка. За 30-40 минут дистилляции в вашем кокосовом бокале будет уже 350 миллилитров пресной воды.
Бедный Робинзон
Какие спички, какой костер! Только ты и вокруг дикая природа. Ну, и немного подручных средств.
Всеми правдами и неправдами находим бутылку или иной сосуд, в который будет скапливаться пресная вода, целлофановую пленку или пакет. И переходим к рытью ямки в нескольких метрах от береговой линии. Копаем до тех пор пока вода не просочится из под земли.
У бутылки отрезаем верхнюю часть и, перевернув вниз горлышком, вставляем ее в нижнюю. Благодаря такой конструкции вода будет стекать в сосуд, но при этом не будет испаряться обратно.
Помещаем бутылку в центр ямы. Сверху ямку застилаем целлофановой пленкой. А в центр пленки, ровно под бутылкой, кладем грузик в виде камня и горсти земли. Испаряясь, капли воды будут конденсироваться на пленке и под собственным весом скатываться по продавленной пленке точно в наш сосуд.
Если по каким-то причинам нам так и не удалось докопаться до воды, то не отчаиваемся. Заполняем выкопанную яму зеленью, травой, листьями растений и так же накрываем пленкой. Парниковый эффект испарит из них бесценную влагу. Главное, чтобы солнце не подвело.
Единственный нюанс: так как конденсат абсолютно лишен солей, опытные экстремалы советуют добавить немного морской воды. Это позволит быстрей утолить жажду.
Сетевое издание TechInsider
Учредитель ООО «Фэшн Пресс»: 119435, г. Москва, Большой Саввинский пер., д. 12, стр. 6, этаж 3, пом. II;
Адрес редакции: 119435, г. Москва, Большой Саввинский пер., д. 12, стр. 6, этаж 3, пом. II;
Главный редактор: Василенок Никита Александрович
Адрес электронной почты редакции: info@techinsider.ru
Номер телефона редакции: +7 (495) 252-09-99
Знак информационной продукции: 16+
Cетевое издание зарегистрировано Федеральной службой по надзору в сфере связи, информационных технологий и массовых коммуникаций, регистрационный номер и дата принятия решения о регистрации: серия ЭЛ № ФС 77 — 84123 от 09 ноября 2022 г.
© 2007 — 2023 ООО «Фэшн Пресс»
При размещении материалов на Сайте Пользователь безвозмездно предоставляет ООО «Фэшн Пресс» неисключительные права на использование, воспроизведение, распространение, создание производных произведений, а также на демонстрацию материалов и доведение их до всеобщего сведения.
Источник