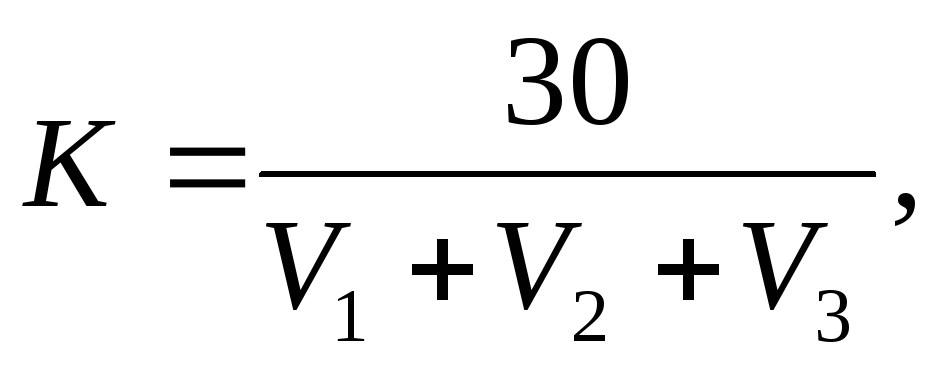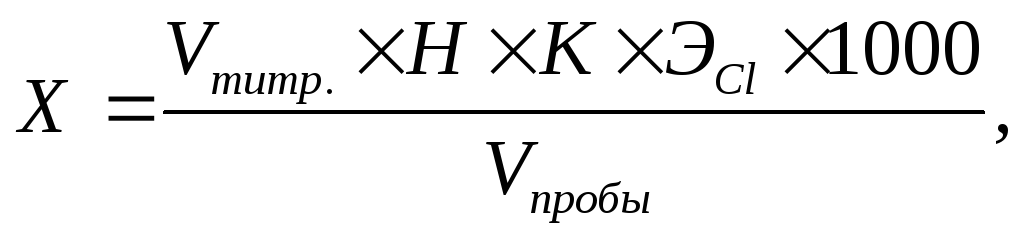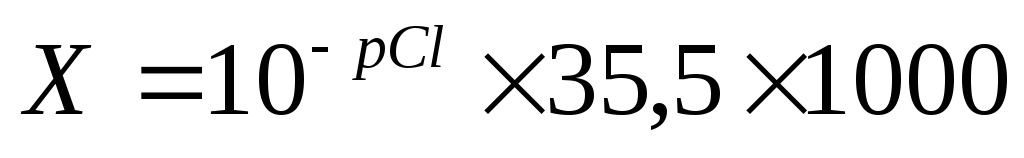Метод Мора
Метод основан на том, что галиды (хлориды, бромиды, иодиды) с ионом серебра дают практически нерастворимый галид серебра, выпадающий в осадок. Рабочий титрованный раствор — раствор AgNO3. Для определения конца реакции пользуются хроматом калия К2Сг04. В этом случае протекают две реакции:
Обе получающиеся соли — AgCl и Ag2Cr04 — трудно растворы в воде, но при добавлении AgNO3 к раствору, содержащему, кроме ионов Сl — , также ионы СlO4 2- первоначально образуется AgCl и только потом, когда ионы Сl — практически полностью будут удалены из раствора, начинается образование Ag2CrO4. В этот момент цвет осадка начнет изменяться: из белого или желтого он будет переходить в [красноватый, по появлению которого и судят о том, что реакция между ионами Сl — и Ag + закончилась. Такая последовательность образования осадков зависит от того, что AgCl менее растворим (1,25-10 г-экв/л), чем Ag2Cr04 (0,65-10 г-экв/л), и потому осаждается из раствора первым.
Применение метода Мора ограничено: точные результаты получаются только в нейтральной среде. В минеральных кислотах Ag2Cr04 растворяется и в их Присутствии выпадать не может. В присутствии щелочей метод Мора также не применим, так как в таких растворах ионы ОН — дают с ионами Ag + бурый осадок Ag2O, который образуется вследствие распада получающейся неустойчивой гидрида серебра:
В аммиачной среде осадки AgCl и Ag2Cr04 растворяются, что обусловлено образованием комплексных аммиачно-серебряных солей. Не применим этот метод также в присутствии ионов Ba 2+ , Pb 2+ и всех остальных ионов, которые дают не растворимые в воде осадки с ионами CrO4 2- .
Титрование по Мору следует производить при комнатной температуре, так как с повышением температуры увеличивается произведение растворимости Ag2CrO4 2- ; вследствие этого уменьшается чувствительность индикатора к иону Ag + .
Метод Фольгарда
Метод основан на образовании не растворимого в воде роданида серебра AgCNS, имеющего белый цвет. В качестве рабочих титрованных растворов применяют раствор нитрата серебра AgNO3 и раствор роданида калия КCNS или аммония NН4CNS, применимым в нейтральной и кислой среде. Наличие в растворе свободной кислоты дает более точный результат. Конец осаждения определяют индикаторами. В качестве индикатора применяют железо – аммиачные квасцы NН4Fe(SO4)2∙12H2O, которые в виде насыщенного раствора прибавляются к титруемой жидкости. Протекает реакция:
Как только реакция между ионами Ag и CNS заканчивается, следующая капля роданида калия вызывает образование роданида железа, который окрашивает жидкость в красный цвет
Для приготовления железо-аммиачных квасцов, нагревают насыщенный раствор, дают раствору охладится, затем фильтруют. К профильтрованной жидкости прибавляют концентрированную азотную кислоту до тех пор , пока она не станет бесцветной.
Лабораторная работа
Опыт 1 . Определение хлорида натрия по Мору.
Выполнение работы. На аналитических весах точно отвесить 1,4598г хлорида натрия (на 250 мл воды). Навеску перенести в мерную колбу растворить навеску в дистиллированной воде и довести до 250 мл. Отмерить пипеткой 20мл приготовленного раствора, прибавить 0,5 мл 5% раствора КCr04 и титровать из бюретки рабочим раствором AgNO3. По результатам титрования вычислить процентное содержание соли в пробе.
Определить нормальность приготовленного раствора хлорида натрия:
Содержание в навеске определяем по формуле:
Опыт 2. Определение хлорида натрия по Фольгарду
Выполнение работы. На аналитических весах точно отвесить навеску NaCl (m1=0,5798г) таким образом, чтобы получился 0,1н раствор. Из приготовленного раствора взять 25 мл, перенести в коническую колбу на 200мл и прилить из бюретки точно отмеренный объем титрованного раствора AgNO3. Объем раствора АgNO3 должен быть в 2 раза больше, чем нужно для полного осаждения ионов Cl — . Образуется осадок AgCl, а некоторая часть AgNO3 остается в свободном состоянии. Колбу с мутной жидкостью сильно встряхивают до тех пор пока AgCl не свернется, образуя комки и не осядет на дно. Жидкость становится прозрачной. Прибавляют 2-3 мл железо –аммиачных квасцов и оттитровывают избыток нитрата серебра NН4CNS до появления красноватого окрашивания не исчезающего при сильном взбалтывании. Расчет проводят по формулам. V1 AgNO3–объем прилитого раствора AgNO3
Источник
Лабораторная работа № 20 Аргентометрическое определение хлоридов по методу Мора
Сущность метода.Метод Мора основан на осаждении хлоридов азотнокислым серебром в присутствии хромата калияK2CrO4. Нитрат серебра при наличии в растворе хлоридов первоначально реагирует с ними, а лишь затем после связывания всех хлоридов образуется хромат серебра оранжево-красного цвета.
Реактивы и оборудование
Нитрат серебра, раствор 0,01 моль-экв/дм 3
Хлорид натрия, раствор 0,01 моль-экв/дм 3
Конические колбы для титрования
Ход определения
При содержании хлоридов менее 250 мг/дм 3 берут 100 см 3 фильтрованной испытуемой воды. При большем содержании хлоридов берут 10 – 50 см 3 исследуемой воды и разбавляют до 100 см 3 дистиллированной водой. В две конические колбы для титрования вносят по 100 см 3 анализируемой воды, прибавляют по 5 капель раствораK2CrO4. Раствор в одной колбе титруют 0,01 Н AgNO3 до изменения окраски раствора по сравнению с окраской во второй колбе (цветной свидетель).
Стандартизация титранта. Для стандартизации титранта в коническую колбу вносят 10 см 3 0,01 Н раствораNaCд и 90 см 3 дистиллированной воды, прибавляют 5 капельK2CrO4. Содержимое колбы титруют 0,01 Н растворомAgNO3до перехода лимонно-желтой окраски мутного раствора в оранжево-красную, не исчезающую в течение 15 – 20 сек.
Поправочный коэффициент к титруAgNO3рассчитывают по результатам трех титрований
где V1, V2, V3 – объемы AgNO3, пошедшие на каждое из трех титрований, см 3 .
Расчет. Содержание хлорид-иона Х (мг/дм 3 ) рассчитывают по формуле:
где Vтитр. – количество раствора AgNO3, пошедшее на титрование, см 3 ;
Н – концентрация титранта – нитрата серебра, моль-экв/дм 3 ;
К – поправочный коэффициент к концентрации титранта;
ЭCl – эквивалент хлорид-иона, г/моль-экв;
Vпробы – объем воды, взятой для анализа, см 3 ;
1000 – коэффициент для перехода от граммов к миллиграммам.
Лабораторная работа № 21 Определение хлоридов с помощью ионоселективного электрода
Сущность метода.Потенциометрический метод определения хлоридов основан на определении ЭДС электродной системы, состоящей из хлоридного ионоселективного электрода и вспомогательного хлоридсеребряного электрода. Он позволяет определить суммарную концентрацию хлоридов (всех его форм: иона хлора, его комплексных соединений). Метод используется для растворов с концентрацией хлоридов 0,1 – 10,0 мг/дм 3 .
Мешающие вещества. Мешают большие количества сульфидов, хлоридов, бромидов, роданидов, образующих на поверхности электрода нерастворимые соли, а также сильные восстановители и вещества, образующие комплексные соединения с серебром (например, ЭДТА).
Реактивы и оборудование
Иономер с иононоселективным хлоридным и хлоридсеребрянным электродами
Хлорид натрия, 0,1 М раствор.
Ацетатный буферный раствор
Ход определения.
Построение градуировочного графика. Из основного стандартного раствора хлорида натрия с концентрацией 0,1 М методом последовательного десятикратного разбавления готовят растворы 10 -2 М, 10 -3 М,10 -4 М, 10 -5 М, для чего 10 см 3 раствора с более высокой концентрацией наливают в колбу на 100 см 3 и доводят водой до метки. Полученные растворы имеют значения рCl= 1, 2, 3, 4, 5. В стакан вместимостью 50 см 3 вливают 20,0 см 3 рабочего стандартного раствора с рCl= 5, приливают 5 см 3 ацетатного буферного раствора, перемешивают на магнитной мешалке. Измеряют ЭДС при перемешивании раствора магнитной мешалкой. Аналогично измеряют ЭДС для других стандартных растворов. При выполнении измерений необходимо следить за тем, чтобы на поверхности мембраны хлоридного электрода не налипали пузырьки воздуха.
По результатам измерений строят градуировочный график зависимости значение ЭДС, милливольты – значение рCl.
Определение хлоридов в анализируемой воде. В стакан вместимостью 50 см 3 помещают 20 см 3 анализируемой воды (температура воды не должна отличаться от температуры стандартных растворов, по которым калибруют электрод, более чем на2 0 С, в противном случае воду следует подогреть или охладить). Затем помещают в раствор магнит от магнитной мешалки, приливают 5 см 3 буферного раствора и погружают в раствор тщательно промытые дистиллированной и анализируемой водой ионоселективный хлоридный и вспомогательный электроды. Измеряют ЭДС. По градуировочному графику находят значение рClанализируемой воды.
Расчет.Концентрация хлоридов в воде (Х) вмг/дм 3 рассчитывается по формуле:
,
где рСl– показатель концентрации хлорид-иона; найденный по графику;
35,5– молярная масса иона хлора, г/моль;
1000 – коэффициент для перехода от граммов к миллиграммам.
Источник