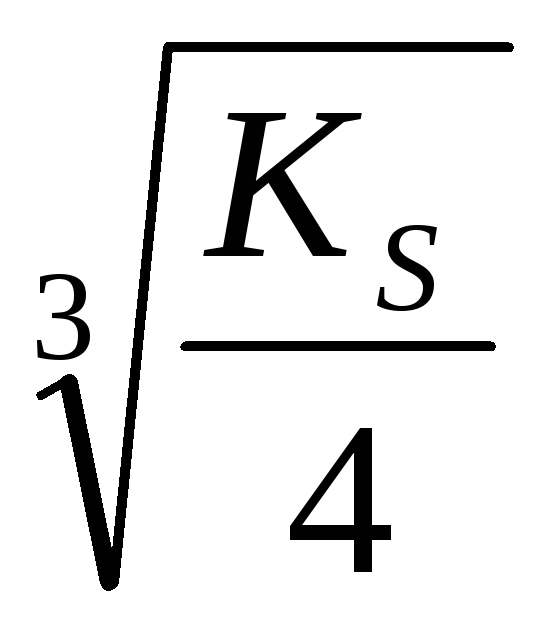Метод Мора
Метод основан на том, что галиды (хлориды, бромиды, иодиды) с ионом серебра дают практически нерастворимый галид серебра, выпадающий в осадок. Рабочий титрованный раствор — раствор AgNO3. Для определения конца реакции пользуются хроматом калия К2Сг04. В этом случае протекают две реакции:
Обе получающиеся соли — AgCl и Ag2Cr04 — трудно растворы в воде, но при добавлении AgNO3 к раствору, содержащему, кроме ионов Сl — , также ионы СlO4 2- первоначально образуется AgCl и только потом, когда ионы Сl — практически полностью будут удалены из раствора, начинается образование Ag2CrO4. В этот момент цвет осадка начнет изменяться: из белого или желтого он будет переходить в [красноватый, по появлению которого и судят о том, что реакция между ионами Сl — и Ag + закончилась. Такая последовательность образования осадков зависит от того, что AgCl менее растворим (1,25-10 г-экв/л), чем Ag2Cr04 (0,65-10 г-экв/л), и потому осаждается из раствора первым.
Применение метода Мора ограничено: точные результаты получаются только в нейтральной среде. В минеральных кислотах Ag2Cr04 растворяется и в их Присутствии выпадать не может. В присутствии щелочей метод Мора также не применим, так как в таких растворах ионы ОН — дают с ионами Ag + бурый осадок Ag2O, который образуется вследствие распада получающейся неустойчивой гидрида серебра:
В аммиачной среде осадки AgCl и Ag2Cr04 растворяются, что обусловлено образованием комплексных аммиачно-серебряных солей. Не применим этот метод также в присутствии ионов Ba 2+ , Pb 2+ и всех остальных ионов, которые дают не растворимые в воде осадки с ионами CrO4 2- .
Титрование по Мору следует производить при комнатной температуре, так как с повышением температуры увеличивается произведение растворимости Ag2CrO4 2- ; вследствие этого уменьшается чувствительность индикатора к иону Ag + .
Метод Фольгарда
Метод основан на образовании не растворимого в воде роданида серебра AgCNS, имеющего белый цвет. В качестве рабочих титрованных растворов применяют раствор нитрата серебра AgNO3 и раствор роданида калия КCNS или аммония NН4CNS, применимым в нейтральной и кислой среде. Наличие в растворе свободной кислоты дает более точный результат. Конец осаждения определяют индикаторами. В качестве индикатора применяют железо – аммиачные квасцы NН4Fe(SO4)2∙12H2O, которые в виде насыщенного раствора прибавляются к титруемой жидкости. Протекает реакция:
Как только реакция между ионами Ag и CNS заканчивается, следующая капля роданида калия вызывает образование роданида железа, который окрашивает жидкость в красный цвет
Для приготовления железо-аммиачных квасцов, нагревают насыщенный раствор, дают раствору охладится, затем фильтруют. К профильтрованной жидкости прибавляют концентрированную азотную кислоту до тех пор , пока она не станет бесцветной.
Лабораторная работа
Опыт 1 . Определение хлорида натрия по Мору.
Выполнение работы. На аналитических весах точно отвесить 1,4598г хлорида натрия (на 250 мл воды). Навеску перенести в мерную колбу растворить навеску в дистиллированной воде и довести до 250 мл. Отмерить пипеткой 20мл приготовленного раствора, прибавить 0,5 мл 5% раствора КCr04 и титровать из бюретки рабочим раствором AgNO3. По результатам титрования вычислить процентное содержание соли в пробе.
Определить нормальность приготовленного раствора хлорида натрия:
Содержание в навеске определяем по формуле:
Опыт 2. Определение хлорида натрия по Фольгарду
Выполнение работы. На аналитических весах точно отвесить навеску NaCl (m1=0,5798г) таким образом, чтобы получился 0,1н раствор. Из приготовленного раствора взять 25 мл, перенести в коническую колбу на 200мл и прилить из бюретки точно отмеренный объем титрованного раствора AgNO3. Объем раствора АgNO3 должен быть в 2 раза больше, чем нужно для полного осаждения ионов Cl — . Образуется осадок AgCl, а некоторая часть AgNO3 остается в свободном состоянии. Колбу с мутной жидкостью сильно встряхивают до тех пор пока AgCl не свернется, образуя комки и не осядет на дно. Жидкость становится прозрачной. Прибавляют 2-3 мл железо –аммиачных квасцов и оттитровывают избыток нитрата серебра NН4CNS до появления красноватого окрашивания не исчезающего при сильном взбалтывании. Расчет проводят по формулам. V1 AgNO3–объем прилитого раствора AgNO3
Источник
Метод Мора
Индикатором служит хромат – ион, который образует красно-кирпичный осадок Ag2CrO4, более растворимый, чем AgCl. При титровании Ag2CrO4 не выпадет, пока Cl — не будет оттитрован полностью.
(S(Ag2CrO4) = = 6,5 * 10 -5 M, S(AgCl) = 1,3 * 10 -5 M).
На практике создают концентрацию CrO4 2- равную от 0,35 М до 1,1*10 -4 .
6 Расчёт индикаторных погрешностей
При титровании с индикатором CrO4 2- раствор перетитровывается. В конечной точке титрования концентрация Cl — складывается из C0( f-1) и ионов, поступающих за счет частичного растворения AgCl.
[Cl — ]KTT =
ПТ = f-1 = 
Как видно, систематическая погрешность тем меньше, чем меньше чем больше концентрация титруемого вещества и титранта и чем больше КТТ к точке эквивалентности.
Ag2CrO4 2 Ag + + CrO4 2-
[Ag + ] = = 6,5 * 10 -5
ПТ = = 6,2 * 10 -4
ПТ, 
7 Вывод по кривой титрования.
1)В осадительном титровании наблюдается одна точка эквивалентности,
pCl в точке эквивалентности рассчитывается по формуле
pCl = P KS
Кривая симметрична относительно точки эквивалентности.
2) Кривые осадительного титрования относятся к монологарифмическим кривым.
3) Скачок титрования составляет pCl от 3,0 до 6,74
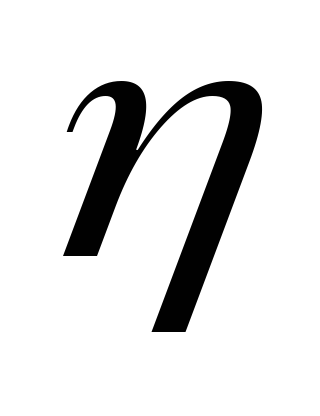


4) Чем меньше произведение растворимости осадка и больше исходная концентрация, тем больше скачок титрования и индекс крутизны, а следовательно, тем меньше стандартное отклонение результатов титрования.
Источник