9.1. Аргентометрия
Основными рабочими растворами аргентометрии являются растворы нитрата серебра, хлорида натрия и тиоцианата калия или аммония. Хранят раствор AgNO3 в склянках из темного стекла, так как на свету соли серебра неустойчивы. Точную концентрацию раствора AgNO3 обычно устанавливают по хлориду натрия.
Растворы NaCl KSCN (NH4SCN) готовят из перекристаллизованных препаратов. Точную концентрацию KSCN (или NH4SCN) устанавливают по титрованному раствору нитрата серебра.
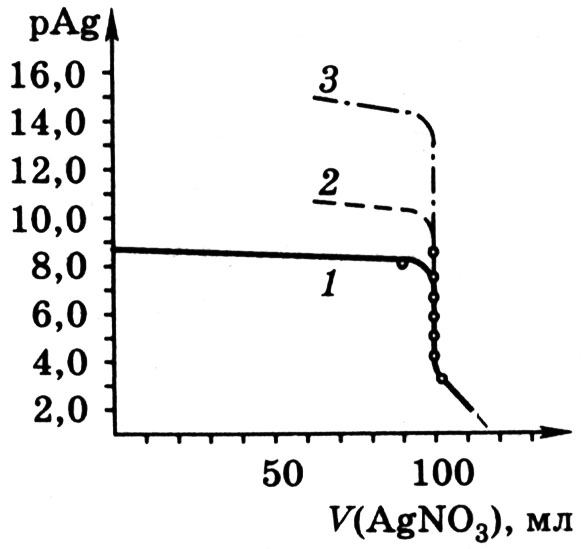
Кривые титрования в аргентометрии строят обычно в координатах pAg – V, где pAg = — lg[Ag + ], V – объем титранта.
Рассчитаем, например, кривую титрования 100,0 мл 0,10 М раствора NaCl раствором 0,10 М AgNO3, принимая для простоты расчетов, что объем раствора при титровании не изменяется и разница между активностью и концентрацией ионов несущественна.
В водном растворе хлорид натрия диссоциирован нацело, поэтому концентрация хлорид-ионов в начальной точке кривой титрования, равна концентрации NaCl, т.е. 0,10 моль/л и рCl = 1,00.
Добавление 1,00 мл раствора AgNO3 к NaCl вызовет образование осадка AgCl и концентрация Cl – в растворе уменьшится. Равновесные концентрации ионов в растворе будут равны: [Ag + ] = x, [Cl – ] = 0/099 + x. В соответствии с правилом произведения растворимости [Ag + ] [Cl – ] = 1,78·10 -10 можно записать
х(х +0,099) = 1,78·10 -10 , откуда х = [Ag + ] = моль/л или
рAg = 8,74. Добавление 90,0 мл раствора AgNO3 свяжет примерно 90 % хлорида в осадок AgCl, и в растворе останутся равновесные концентрации [Ag + ] = х и [Cl – ] = 0,01 + х. Из ПРAgCl получаем: х = [Ag + ] = моль/л, что соответствует рAg = 6,74. После добавления 99,9 мл раствора AgNO3 в анализируемом растворе останется примерно 0,1 % взятого для титрования количества хлорида, т.е. в растворе будет [Ag + ] – х, [Cl — ] = 10 -4 + х и х = = 1,78·10 -6 моль/л, откуда рAg = 5,74. При добавлении 100,0 мл раствора AgNO3 достигается точка эквивалентности, в которой концентрации ионов Ag + и Сl — одинаковы:
[Ag + ] =[Cl — ] = = 1,33·10 -5 моль/л, а рAg = 4,88. Избыток в 0,10 мл раствора AgNO3 сверх эквивалентного приводит к концентрации [Ag + ] =10 -4 +х и [Cl — ] = х, а так как х « 1,0·10 -4 , то [Ag + ] = 1,0·10 -4 моль/л, и рAg = 4,0. Избыток в 1,00 мл раствора AgNO3 дает [Ag + ] = 1,0·10 -3 моль/л и рAg = 3. Кривая аргентометрического титрования представлена на рис. 9.1.
Рис. 9.1. Кривые аргентометрического титрования
Как показывает рисунок кривая сохраняет традиционный вид. Сначала от первых капель до оттитровывания 90 % имеющегося хлорида рAg изменяется всего на одну единицу, затем то же изменение рAg вызывает только 9,0 мл раствора AgNO3, а в области точки эквивалентности наблюдается скачок титрования. Добавление 0,2 мл раствора AgNO3 в этой области (от 99,9 до 100,1 мл) вызывает изменение рAg от 5,74 до 4,00, т.е. почти на две единицы. Величина скачка титрования возрастает с увеличением концентрации реагирующих веществ и с уменьшением температуры, так как понижение температуры вызывает уменьшение ПР. Зависимость величины скачка титрования от ПР можно проследить, если рассчитать область скачка титрования для реакции взаимодействия AgNO3 с бромидом и иодидом натрия. С уменьшением ПР соли серебра, образующейся при титровании, увеличивается скачок титрования (рис. 9.1).
Установление точки эквивалентности в аргентометрии осуществляется как с помощью индикаторов, так и без них, следующими методами.
1. Метод равного помутнения
Метод равного помутнения предложен Гей-Люссаком и характеризуется высокой точностью. При титровании, например, хлорида натрия нитратом серебра вблизи точки эквивалентности отбирают небольшие порции прозрачного раствора и добавляют к одной порции AgNO3, а к другой NaCl. Если точка эквивалентности достигнута, то помутнение в обеих порциях будет одинаковым. В недотитрованных растворах помутнение будет происходить только при добавлении AgNO3, а в перетитрованных – при добавлении NaCl.
2. Метод Мора (индикатор – хромат калия)
Идея метода основана на образовании кирпично-красного осадка хромата серебра Ag2CrO4 в точке конца титрования. При аргентометрическом титровании хлорида концентрация ионов в точке эквивалентности составляет
[Ag + ] =[Cl — ] = = = 1,33·10 -5 моль/л. Концентрация ионов CrO4 2– , необходимая для достижения , при этой концентрации ионов Ag + составляет [CrO4 2– ] = моль/л, однако при этой концентрации осадок хромата серебра «на глаз» не будет заменен. Для визуального обнаружения осадка хромата серебра обычно бывает достаточно перетитровать анализируемый раствор на одну каплю раствора AgNO3.
Титрование с хроматом калия в качестве индикатора проводится в нейтральной или слабощелочной среде, когда рН раствора больше 6,5, но меньше 10,5. В более кислой области происходит протонирование хромата (CrO4 2– + H + = HCrO4 – ) и чувствительность индикатора падает, а при рН > 10,5 оксид или гидроксид серебра может выпадать ранее хромата.
Метод Мора обычно применяют для определения хлоридов и бромидов. Иодиды и тиоцианаты так не определяются, в связи с тем, что вследствие адсорбции установление точки эквивалентности становится затруднительным и погрешность анализа существенно возрастает.
3. Метод Фольгарда [индикатор – тиоцианатные комплексы железа (III)]
Реакцию взаимодействия серебра с тиоцианатом используют для определения галогенидов методом обратного титрования. По этому методу к анализируемому раствору галогенида (хлорида или бромида) добавляют избыток титрованного раствора AgNO3 и не вошедшее в реакцию количество Ag + оттитровывают тиоцианатом калия или аммония в присутствии ионов Fe 3+ .
Тиоцианатная реакция железа позволяет обнаружить в растворе тиоционат при концентрации порядка 10 -5 моль/л, что соответствует 0,01 мл 0,1 М KSCN в 100,0 мл раствора.
В точке эквивалентности [Ag + ] =[SCN – ] = = 1,05·10 –6 . При этой концентрации тиоцианата окрашивание раствора не происходит. Первая же избыточная капля тиоцианата калия (аммония) вызывает четкую оранжевую окраску.
По методу Фольгарда можно оттитровать и другие анионы, образующие малорастворимые соединения с ионами Ag + (CrO4 2- , PO4 3- и др.). Достоинством метода Фольгарда является возможность определения галогенидов в кислой среде.
4. Метод Фаянса (адсорбционные индикаторы)
Адсорбционными индикаторами называют соединения, которые при адсорбции на осадке изменяют свой цвет. Установлено, что в первую очередь на осадке адсорбируются ионы, одноименные с осадком. Например, при титровании хлорида нитратом серебра на осадке AgCl до точки эквивалентности будут адсорбироваться преимущественно ионы Cl – и для нейтрализации отрицательного заряда к частицам осадка будут притягиваться положительно заряженные ионы из раствора. После точки эквивалентности адсорбироваться на осадке будут избыточные ионы Ag + и для нейтрализации положительного заряда осадка из раствора будут притягиваться отрицательно заряженные ионы, в том числе анионы индикатора. Анионы некоторых красителей, адсорбируясь, изменяют свой цвет. Так, флуоресцин, применяемый при титровании хлоридов, в растворе имеет желто-зеленую окраску, а в точке эквивалентности окрашивает осадок AgCl в красный цвет. Для титрования бромидов, иодидов и тиоцианатов используют эозин: в точке эквивалентности окраска из желтой становится розовой.
Метод Фаянса имеет менее широкое применение, чем методы Мора и Фольгарда.
Источник
Метод Мора
Метод Мора является одним из аргентометрических методов. Все эти методы основаны на реакции:
Метод Мора является наиболее простым из всех методов аргентометрии и в то же время достаточно точным. Титрантом является раствор нитрата серебра АgNОз 0.1 моль/л.
В основу метода Мора положена реакция взаимодействия ионов серебра с С1 — или Вг — .
Индикатором является хромат калия К2СгО4 5 %. Установочным веществом для определения титра раствора является NаС1 или КС1 0.1 моль/л.
Метод Мора позволяет определить количество хлоридов или бромидов. Иодиды этим методом не определяют, так как выпадающий в осадок иодид серебра АgI сильно адсорбирует К2СгО4, поэтому точку эквивалентности определить невозможно.
Растворимость АgСl значительно меньше, чем растворимость Аg2СгO4. Поэтому если постепенно добавлять раствор АgNOз к раствору, содержащему Сl — и CrO4 2- , то ПРAgС| достигается раньше ПР Аg2СгO4.
Это означает, что вначале образуется труднорастворимая соль
После того как хлорид-ионы будут практически полностью выделены в виде АgС1, появляется осадок. Происходит изменение окраски титруемой смеси и таким образом определяется конец титрования.
При титровании раствора бромида происходит аналогичное явление. Так как ПРАgВг < ПРАg2СгO4.,то вначале происходит образование АgВг и только после полного выделения АgВг появляется осадок Аg2СгО4, меняющий окраску титруемой смеси. Осадок хромата серебра Аg2СгО4 имеет кирпично- красный цвет. Однако такой цвет можно наблюдать в сильно перетитрованном растворе. В действительности надо титровать только до ясно заметного перехода лимонно-желтой окраски в желто — розовую. Для лучшего определения конца титрования можно использовать раствор «свидетель».
Применение метода Мора ограничено следующими условиями:
1. Определение можно проводить только в нейтральной среде, так как в кислой среде хромат серебра растворяется, и мы не сможем заметить конец титрования. В щелочной среде титрование невозможно потому, что будет выпадать осадок оксида серебра:
2. Определение нельзя проводить в присутствии ионов Ва 2+ , Вi 3+ , Рb 2+ , так как эти ионы образуют с ионами СгО4 2 — осадки.
3. Титрование всегда ведут от галогенида к АgNOз (т. е. галогенид титруют раствором АgNОз, а не наоборот). Только при таком условии кирпично-красный осадок Аg2СгО4 образуется в точке эквивалентности.
Метод Мора находит широкое применение при анализе пищевых продуктов. Количество поваренной соли в колбасе, соленой рыбе, масле и других продуктах определяют по методу Мора.
Этот метод применяется также для определения хлоридов в воде. Метод Мора используется и при анализе некоторых фармацевтических препаратов, например хлоридов и бромидов натрия и калия.
Определение хлоридов методом Мора
Приготовление титранта 0.05 моль/л раствора. Нитрат серебра не относится к тем веществам, из которых можно приготовить раствор заданной концентрации по точно взятой навеске. Поэтому готовят раствор примерно требуемой концентрации, а его титр устанавливают. Необходимую навеску (8.5 г AgNОз на 1 л раствора) отвешивают с точностью до 0.1 г на технических весах, и нужное количество воды отмеривают мерным цилиндром. Раствор сохраняют в темноте, так как на свету нитрат серебра разлагается. Однако и при надлежащем хранении титр раствора АgNОз меняется с течением времени и его необходимо время от времени проверять.
Приготовление установочного раствора. Для приготовления 0.05 моль/л, раствора NаС1 отвешивают на аналитических весах 0.2922 г NаС1 и количественно переносят в мерную колбу вместимостью 100 мл. Растворяют навеску в дистиллированной воде, доводят раствор до метки и хорошо перемешивают. Таким образом получают раствор NаС1.
Определение титра нитрата серебра. В качестве индикатора применяют 5 % раствор хромата калия К2СгО4 в воде. Наполняют бюретку раствором нитрата серебра АgNОз. Отобрав пипеткой 10 мл 0.05 моль/л раствора NаС1, переносят ее в колбу Эрленмейера вместимостью 250 мл, добавляют 0.5 мл раствора индикатора, немного разбавляют водой и медленно титруют 0.1 моль/л раствором АgNОз, непрерывно перемешивая жидкость до появления первого неисчезающего изменения цвета суспензии. Нужно уловить момент, когда лимонно-желтый цвет суспензии приобретет от капли АgNОз слегка красноватый оттенок. Запись анализа и расчеты производят так же, как при определениях кислотно-основным методом.
Определение хлорида в растворе. Раствор хлорида помещают в мерную колбу на 100 мл, доводят дистиллированной водой до метки и перемешивают. Для титрования отбирают в коническую колбу 10 мл полученного раствора, немного разбавляют водой, добавляют 0.5 мл раствора К2СгO4 и титруют раствором АgNОз до изменения окраски содержимого колбы из лимонно-желтой в желто-розовую. Рассчитывают содержание хлора в полученном растворе (в граммах).
Понравилась статья? Добавь ее в закладку (CTRL+D) и не забудь поделиться с друзьями:
Источник