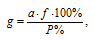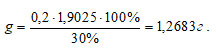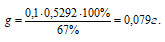- Лабораторная работа
- Гравиметрическое определение вещества в навеске сплава алюминия и соли Мора
- Гравиметрическое определение сульфата железа в навеске соли Мора
- Гравиметрическое определение алюминия в навеске его сплава
- Гравиметрический метод соль мора
- Определение железа в растворе соли Мора
- Гравиметрическое определение вещества в навеске сплава алюминия и соли Мора
- Гравиметрическое определение сульфата железа в навеске соли Мора
- Гравиметрическое определение алюминия в навеске его сплава
- Анализ технической соли Мора
Лабораторная работа
Для перманганатометрических определений рекомендуется применять 0,02 н. раствор КМnO4, т.е. содержащий 0,02 г — экв в 1 л. Поскольку титрование перманганатом производят в кислой среде, то ЭKMnO4=31,61 г. Это весовое количество КМnO4 должно находиться в 1 л 1 н. раствора. Так как нам нужен 0,02 н. раствор перманганата, то для растворения в 1 л. надо взять 0,02 г, т.е.
Однако нельзя приготовить титрованный раствор КМnO4, исходя из его точной навески, поэтому установка титра и нормальности КМnO4 обязательна. Это необходимо потому, что в перманганате почти всегда имеется некоторое количество МnO2. Для приготовления раствора отвесить на технических весах около 0,7г сухой соли КМnO4, растворить в 1л воды, хорошо перемешать и оставить на 8-10 дней в склянке из темного стекла, закрытой стеклянной пробкой. Для титрования перманганатом бюретки применяют только со стеклянным краном. Деления в бюретке отсчитывают по верхнему краю мениска. Установление титра и нормальности раствора перманганата по щавелевой кислоте
Выполнение работы. Заполнить бюретку раствором перманганата калия. В колбу для титрования залить 20мл H2SO4 и нагреть до 80-90 0 С. в горячий раствор пипеткой внести 10 мл стандартного раствора Н2С2O4 и титруют перманганатом калия. Сначала обесцвечивание идет медленно, но по мере накопления ионов, обесцвечивание происходит мгновенно. Титруют до появления бледно-розовой окраски, устойчивой в течении 30сек. Титрование проводят 3 раза, нормальность и титр рассчитывают по формуле:
Опыт 2. Определение железа (II) в растворе соли Мора.
Соль Мора представляет собой двойную соль состава:
При взаимодействии соли Мора с перманганатом калия соль закиси железа (Fe 2+ ) окисляется в соли окиси (Fe 3+ ) по уравнению:
Выполнение работы. В мерную колбу емкостью 100 мл возьмите немного соли Мора добавьте дистиллированной воды до метки и хорошо перемешайте. Полученным раствором ополосните пипетку и перенесите 10мл исследуемого раствора в колбу. Добавьте цилиндром 8-10 мл 2н серной кислоты и титруйте перманганатом калия холодный раствор (нагревание способствует окислению Fe 2 + кислородом воздуха до Fe 3+ ). Титрование вести до появления бледно розовой окраски, не исчезающей в течение 1 мин. Повторите титрование не менее 3 раз, возьмите среднее из отчетов и вычислите количество граммов железа в исследуемом растворе.
Вычисление. Нормальность Fe 2 + в соли Мора вычислите по затраченным на титрование объемом растворов (нормальность KMnO4 известна из предыдущей работы ). Умножив нормальность на грамм- эквивалент железа (55,85г) найдете количество железа в 1 л раствора.
Опыт 3. Определение содержания кальция в растворе.
Катион Ca 2+ не отдаёт электронов, не может быть восстановлен и не реагирует с перманганатом калия. поэтому количество его нельзя определять непосредственным титрованием раствора перманганатом. Определение выполняют косвенным методом.
Из анализируемого раствора ионы Ca 2+ осаждают действием щавелевой кислоты или оксалата натрия.
Осадок оксалата кальция отфильтровывают, промывают и обрабатывают горячей разбавленной серной кислотой. При этом в раствор переходит эквивалентное кальцию количество щавелевой кислоты:
Щавелевую кислоту титруют рабочим раствором перманганата калия:
При вычислении надо учитывать, что эквивалент H2C2O4*2H2O в данном случае равен Ѕ грамм- молекулы, а эквивалент Ca 2+ соответственно Ѕ его грамм- атома, т. е 20,04 г.
Выполнение работы. В химический стакан возьмите для анализа немного раствора соли Ca 2+ (около 0,05 г Ca 2+ ). Прибавьте к нему 5- 6 мл 1 н. раствора щавелевой кислоты и нагрейте смесь до кипения. Затем, добавив 2- 3 капли метилового оранжевого медленно нейтрализуйте жидкость аммиаком до перехода красной окраски индикатора в желтую. Содержимому стакана дайте постоять до тех пор, пока осадок оксалата кальция CaC2O4 соберется на дне. Осадок отфильтровывают через синий фильтр, промывают, затем растворяют в серной кислоте разбавляя (1:5) и освободившуюся щавелевую кислоту титруют раствором перманганата калия. Количество перманганата калия, пошедшее на окисление щавелевой кислоты, эквивалентно количеству кальция. Процесс титрования заканчивают с появлением в растворе слабо- малинового цвета, титрование повторяют 2- 3 раза.
Количество Ca 2+ в растворе вычисляют по формуле:
Источник
Гравиметрическое определение вещества в навеске сплава алюминия и соли Мора
Гравиметрическое определение сульфата железа в навеске соли Мора
Задача 52.
Вычислить навеску исследуемого образца, необходимого для получения определенного количества весовой формы. Исследуемый образец: соль Мора; определяемое вещество FeSO4, приблизительное содержание 30 %; весовая форма Fe2O3, масса 0,2г.
Решение:
Расчёт навески вещества в пробе проводим по формуле:
где а — масса весовой формы определяемого вещества, г;
f- аналитический множитель (фактор пересчета);
a — масса навески, г;
Р — приблизительное процентное содержание вещества в образце.
Подставим все числовые значения в расчётную формулу:
Ответ: Для гравиметрического определения FeSO4 необходимо взвесить навеску соли Мора массой близкой к 1,27г.
Гравиметрическое определение алюминия в навеске его сплава
Задача 53.
Вычислить навеску исследуемого образца, необходимого для получения определенного количества весовой формы. Исследуемый образец: алюминиевый сплав; определяемое вещество Al, приблизительное содержание 67%; весовая форма Al2O3, масса 0,1г.
Решение:
Расчёт навески вещества в пробе проводим по формуле:
где а — масса весовой формы определяемого вещества, г;
f- аналитический множитель (фактор пересчета);
a — масса навески, г;
Р — приблизительное процентное содержание вещества в образце.
Ar(Al) = 26,98;
Mr(Аl2O3) = 101,96;
f = 2Ar(Al)/Mr(Аl2O3) = (2 . 26,98)/101,96 = 0,5292.
Подставим все числовые значения в расчётную формулу:
Ответ: Для гравиметрического определения алюминия необходимо взвесить навеску алюминиевого сплава массой близкой к 0,079г.
- Вы здесь:
- Главная
- Задачи
- Аналитическая химия
- Гравиметрический анализ соли Мора и алюминиевого сплава. Задачи 52 — 53
Источник
Гравиметрический метод соль мора
- Главная
- Химия
- Окислительно-восстановительное титрование
- Определение железа в растворе соли Мора
Определение железа в растворе соли Мора
Опыт 2. Определение железа (II) в растворе соли Мора.
Принцип метода. Титрование железа (II) основано на реакции:
5Fe2+ + MnO4-+ 8H+ ® 5Fe3+ + Mn2+ + 4H2O.
Если железо (II) входит в состав соли Мора (NH4)2SO4·FeSO4·6H2O, то идёт следующая реакция:
2KMnO4 + 10(NH4)2SO4·FeSO4 + 8H2SO4 ® 2MnSO4 + 5Fe2(SO4)3 + K2SO4 +
10 5 Fe2+ — e — ® Fe3 + 2 1 MnO4- + 8H+ + 5e — ® Mn2+ + 4H2O
Реагенты и оборудование: стандартизованный 0,05 н раствор перманганата калия; раствор соли Мора; 2 н раствор серной кислоты; бюретка; стеклянная воронка; конические колбы ёмкостью 100 мл; пипетки Мора; стеклянный цилиндр ёмкостью 50 мл; мерная колба ёмкостью 100 мл.
Ход анализа. В мерную колбу ёмкостью 100 мл наливают немного раствора соли Мора, доводят объём дистиллированной водой до метки и перемешивают. Из этого раствора пипеткой Мора отбирают 10,00 мл и переносят в коническую колбу, добавляют 10 мл 2 н раствора серной кислоты. В чистую бюретку заливают раствор перманганата калия и подготавливают к титрованию. Титрование подкисленного раствора соли Мора перманганатом калия проводят на холоде (при нагревании катион железа (II) окисляется кислородом воздуха до катиона железа (III)) до появления бледно-малиновой окраски, не исчезающей при встряхивании в течение 1-2 минут. Повторяют титрование 2-3 раза.
Обработка результатов. Из сходящихся отсчётов берут средний результат титрования и вычисляют массу железа в анализируемом растворе.
.
Масса железа в 100 мл раствора соли Мора равна:
Источник
Гравиметрическое определение вещества в навеске сплава алюминия и соли Мора
Гравиметрическое определение сульфата железа в навеске соли Мора
Задача 52.
Вычислить навеску исследуемого образца, необходимого для получения определенного количества весовой формы. Исследуемый образец: соль Мора; определяемое вещество FeSO4, приблизительное содержание 30 %; весовая форма Fe2O3, масса 0,2г.
Решение:
Расчёт навески вещества в пробе проводим по формуле:
где а — масса весовой формы определяемого вещества, г;
f- аналитический множитель (фактор пересчета);
a — масса навески, г;
Р — приблизительное процентное содержание вещества в образце.
Подставим все числовые значения в расчётную формулу:
Ответ: Для гравиметрического определения FeSO4 необходимо взвесить навеску соли Мора массой близкой к 1,27г.
Гравиметрическое определение алюминия в навеске его сплава
Задача 53.
Вычислить навеску исследуемого образца, необходимого для получения определенного количества весовой формы. Исследуемый образец: алюминиевый сплав; определяемое вещество Al, приблизительное содержание 67%; весовая форма Al2O3, масса 0,1г.
Решение:
Расчёт навески вещества в пробе проводим по формуле:
где а — масса весовой формы определяемого вещества, г;
f- аналитический множитель (фактор пересчета);
a — масса навески, г;
Р — приблизительное процентное содержание вещества в образце.
Ar(Al) = 26,98;
Mr(Аl2O3) = 101,96;
f = 2Ar(Al)/Mr(Аl2O3) = (2 . 26,98)/101,96 = 0,5292.
Подставим все числовые значения в расчётную формулу:
Ответ: Для гравиметрического определения алюминия необходимо взвесить навеску алюминиевого сплава массой близкой к 0,079г.
Источник
Анализ технической соли Мора

Практические расчеты на срез и смятие При изучении темы обратите внимание на основные расчетные предпосылки и условности расчета.
Функция спроса населения на данный товар Функция спроса населения на данный товар: Qd=7-Р. Функция предложения: Qs= -5+2Р,где.

Аальтернативная стоимость. Кривая производственных возможностей В экономике Буридании есть 100 ед. труда с производительностью 4 м ткани или 2 кг мяса.

Вычисление основной дактилоскопической формулы Вычислением основной дактоформулы обычно занимается следователь. Для этого все десять пальцев разбиваются на пять пар.
Типовые примеры и методы их решения. Пример 2.5.1. На вклад начисляются сложные проценты: а) ежегодно; б) ежеквартально; в) ежемесячно Пример 2.5.1. На вклад начисляются сложные проценты: а) ежегодно; б) ежеквартально; в) ежемесячно. Какова должна быть годовая номинальная процентная ставка.
Выработка навыка зеркального письма (динамический стереотип) Цель работы: Проследить особенности образования любого навыка (динамического стереотипа) на примере выработки навыка зеркального письма.
Словарная работа в детском саду Словарная работа в детском саду — это планомерное расширение активного словаря детей за счет незнакомых или трудных слов, которое идет одновременно с ознакомлением с окружающей действительностью, воспитанием правильного отношения к окружающему.
Концептуальные модели труда учителя В отечественной литературе существует несколько подходов к пониманию профессиональной деятельности учителя, которые, дополняя друг друга, расширяют психологическое представление об эффективности профессионального труда учителя.
Конституционно-правовые нормы, их особенности и виды Характеристика отрасли права немыслима без уяснения особенностей составляющих ее норм.
Толкование Конституции Российской Федерации: виды, способы, юридическое значение Толкование права – это специальный вид юридической деятельности по раскрытию смыслового содержания правовых норм, необходимый в процессе как законотворчества, так и реализации права.
Источник