- Гипотонический раствор морской воды
- Гипертонический и изотонический растворы морской воды для гигиены полости носа: в чем разница?
- Что такое изотонический раствор морской воды?
- Что такое гипертонический раствор?
- Чем отличается гипертонический раствор от изотонического и когда их применять?
- Изотонический раствор
- При снижении осмотического давления крови до 400-350 кПа н аступает гибель организма.
- Давление насыщенного пара растворителя над раствором
Гипотонический раствор морской воды
Гипертонический и изотонический растворы морской воды для гигиены полости носа: в чем разница?
Внутренняя оболочка носа постоянно производит некоторое количество слизи, которая равномерно покрывает слизистую и содержит антисептические вещества. Именно они предохраняют органы дыхания и тем самым весь организм от вредных веществ, которые содержатся во вдыхаемом воздухе. Слизь находится в движении по направлению к глотке благодаря работе множества микроскопических ресничек, покрывающих внутреннюю поверхность носа. Этот механизм нарушается, например, при инфекционных и воспалительных заболеваниях или аллергии — организм получает сигнал о наличии раздражителя, слизистая носа отекает и начинает производить секрет в усиленном режиме. Реснички в свою очередь не могут справиться с ее возросшим количеством, в результате чего возникает скопление слизи и насморк. Отек может спровоцировать застой слизи и, как следствие, такие неприятные заболевания, как гайморит.
Что такое изотонический раствор морской воды?
- нормализует водно-электролитный баланс;
- увлажняет внутреннюю оболочку носа;
- способствует разжижению и выведению слизи;
- питает клетки тканей;
- оказывает противовоспалительный эффект.
Что такое гипертонический раствор?
- уменьшению отека;
- открыванию заблокированных носовых пазух и ходов
- активации местное кровоснабжение
- усиления образования слизи, таким образом ускоряя очищение носовой полости и пазух.
Чем отличается гипертонический раствор от изотонического и когда их применять?
При простуде со слизистыми выделениями из носа как дополнение к лечению можно использовать изотонический раствор с целью очищения слизистой носа перед введением сосудосуживающих спреев от насморка, которые необходимо наносить на очищенную слизистую.
Если речь идет о сильной заложенности носа, застое густой слизи, сложности ее удаления, то решением может стать гипертонический раствор. Аналогичная ситуация и с аллергическими ринитами.
При жидком насморке можно применять изотонический раствор морской воды, а при заложенности или ее чередовании с выделениями — гипертонический.
Регулярное очищение слизистой носа изотоническим раствором морской воды в период цветения растений способствует снижению аллергенной нагрузки на организм за счет своевременного удаления аллергенов со слизистой и тем самым минимизации их попадания в дыхательные пути.
Источник
Изотонический раствор
У животных, которые способны менять количество потребляемой воды в зависимости от обстоятельств, действует особая система осморегуляции. Например, осмолярность мочи бобра, не испытывающего дефицита воды, равна 0,6 осмоль/л, а у живущего в пустыне тушканчика – 9 осмоль/л. У пресноводных рыб тка
невые жидкости гипертоничны по отношению к пресной воде, поэтому такие рыбы накачивают воду путем осмоса через жаберные щели, выводя ее потом из организма с большим объемом разведенной мочи. Напротив, у морских рыб тканевые жидкости гипотоничны по отношению к морской воде, поэтому они через жаберные щели выделяют воду, а для ее компенсации пьют морскую воду. Моча, выделяемая такими рыбами, изотонична морской воде и объем ее очень мал.
При снижении осмотического давления крови до 400-350 кПа н аступает гибель организма.
Онкотическое давление – осмотическое давление, создаваемое за счёт наличия белков в биожидкостях организма. Оно составляет 0,5% от суммарного осмотического давления плазмы крови. В результате понижения онкотического давления при гипопротеинемии происходит перераспределение жидкости в сторону ткани и возникновение онкотических отёков («голодных» или «почечных»).
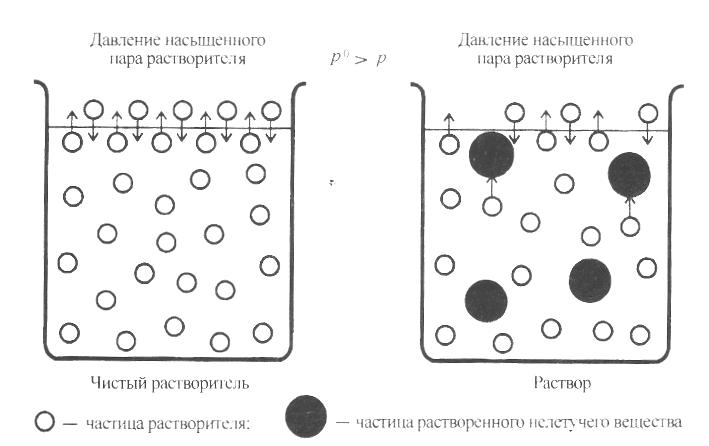
Давление насыщенного пара растворителя над раствором
Д авление насыщенного пара над растворителем (ро) – давление, при котором при данной температуре в системе «жидкость–пар» наступает динамическое равновесие, характеризующееся равенством скоростей испарения и конденсации.
Давление насыщенного Давление насыщенного
пара растворителя р 0 > p пара растворителя
Чистый растворитель Раствор
– частица растворителя; – частица растворенного нелетучего вещества
Рис. 8. Испарение чистого растворителя и испарение растворителя
Если в растворитель ввести нелетучий неэлектролит (рис. 8), то испарение молекул растворителя уменьшится вследствие:
- уменьшения подвижности молекул растворителя за счёт межмолекулярного и ион-дипольного взаимодействия растворитель–вещество;
- уменьшения поверхности испарения, т.к. часть поверхности занята молекулами нелетучего вещества;
- уменьшения молярной доли растворителя и нарушения за счёт этого равновесия жидкость-пар. В соответствии с принципом Ле Шателье начинает протекать процесс, стремящийся ослабить влияние воздействия, т.е. конденсация, что и приводит к уменьшению количества пара, а, следовательно, и к снижению его давления над раствором по сравнению с растворителем.
Давление насыщенного пара растворителя над раствором всегда меньше, чем над чистым растворителем.
Математически это выражается с помощью I закона Рауля.
I закон Рауля – относительное понижение давления насыщенного пара растворителя над раствором в сравнении с его давлением над растворителем, равно молярной доле растворенного вещества (N):
где Ро – давление насыщенного пара над растворителем;
Р – давление насыщенного пара над раствором;
n(X) и n(р-ля) – количество растворенного вещества и растворителя.
Для растворов электролитов в математическое выражение I закона Рауля вводится изотонический коэффициент:
Температуры кипения и кристаллизации растворов непосредственно связаны с давлением над ними насыщенного пара растворителя.
Источник