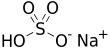Бисульфат натрия в вашем бассейне
Мы неоднократно писали о балансе рН и щелочности в бассейне — в том числе изучая вопрос о том, как понизить эти значения. В данном контексте всегда упоминался и бисульфат натрия. Гидросульфат натрия (NaHSO4), бисульфат натрия или сухая кислота, так называемый pH-минус. Давайте рассмотрим его несколько подробнее и оценим его применимость в вашем бассейне.
Бисульфат натрия, или сухая кислота, является кислотной солью, известной как сульфат водорода натрия. В быту он может использоваться самым разным количеством способов, таких как пищевые добавки или очистка. В бассейнах же чаще всего он используется, чтобы понизить баланс pH и щелочности, когда они становятся слишком высокими.
Обычно химреагент поставляется в виде белого зернистого вещества, кристаллического порошка или гранул, которые могут храниться в контейнере и использоваться по мере необходимости. Конечно же, бисульфат натрия не единственный химикат, который может использоваться, чтобы понизить баланс pH. Соляная кислота также легко справляется с этой задачей и доступна для покупки. Применение HCl допускается ГОСТ-Р-53491.1-2009 «Баccейны: подготовка воды». Использование соляной кислоты в бассейнах с жесткой водой позволяет уменьшить образование малорастворимых солей.
Проблема с соляной кислотой, тем не менее, состоит в том, что это намного более едкое и опасное вещество, которое может сжечь кожу, повредить слизистые, а также и повредить непосредственно бассейновые поверхности, если вы не будете осторожны.
Некоторые люди используют соляную кислоту в очистке плиток и швов удалении различных загрязнений и отложений, поэтому предпочитают также использовать ее же, чтобы при необходимости понизить pH. Но это исключительно «выбор вкуса», если можно так выразиться. Контроль над pH вашего бассейна и уровнями щелочности крайне важен для безопасности на водных объектах. С одной стороны, если любой из упомянутых уровней будет некорректным, применяемый в бассейне хлор не будет в состоянии выполнять свою работу достаточно хорошо. Кроме того, «неуравновешенная» щелочность и уровни рН могут вызвать коррозию или возникновение отложений на оборудовании бассейна, помутнении воды, раздражении на глазах и коже и более быстрому распаду молекул хлора.
Как понизить pH с бисульфатом натрия? Во-первых, вы должны проверить уровни химии всего бассейна удобным вам способом тестирования. Если уровень рН будет слишком высоким, необходимо будет снизить его с бисульфатом натрия.
Большинство продуктов преобразователя pH сделано именно с высокой концентрацией бисульфата натрия — обычно по крайней мере с долей 93.2%. У каждого такого продукта есть свои собственные инструкции для использования, так что крайне важно прочитать их прежде, чем вы попытаетесь использовать его.
Следующий шаг — определить количество бисульфата натрия. Как только вы решили, что pH действительно должен быть уменьшен, необходимо выяснить, сколько бисульфата натрия вы должны добавить.
Большинство экспертов рекомендует применять приблизительно 3/4 из того, к чему призывают инструкции, поскольку остаток всегда можно добавить позже. Затем прочитайте инструкции и узнайте, должен ли ваш продукт быть растворен. Раствор этого соединения имеет pH 1. Обычно гидросульфат сначала растворяют в пластиковом контейнере, а потом добавляют в разные части бассейна. При его использовании в воде увеличивается содержание сульфата. Затем добавьте бисульфат натрия в воду бассейна. Для заглубленного бассейна нужно делать это близко к возвратным форсункам. Для наземного бассейна это актуально около стены. Важно распределить продукт по всему бассейну в течение приблизительно 15 минут, и вы сможете убедиться в его растворении, поскольку он «исчезнет» из вида.
Позвольте продукту работать в течение по крайней мере 6 часов. Не возвращайте пловцов в бассейн, пока вы не сбалансировали воду. После 6 часов повторно проверьте и добавьте дополнительные средства при необходимости.
Как правило, уровни pH и щелочности идут рука об руку. Поэтому важно проверить и уровень щелочности. Обычно если pH будет слишком высоким, щелочность будет слишком низкой. Если щелочность будет слишком низкой, она вызовет ржавление, окрашивание и раздражение глаз и кожи. Уровни рН также будут очень нестабильны в этой ситуации и могут резко колебаться вверх и вниз, что заставляет дезинфицирующее средство терять свою эффективность.
Процесс изменения может быть довольно медленным, так что, вероятно, придется быть терпеливым и продолжать добавлять продукт в течение нескольких дней, чтобы увидеть необходимые изменения.
Чтобы использовать продукт эффективно, убедитесь, что вы прочитали инструкцию. В общем и целом шаги схожи с упомянутыми выше — растворение по необходимости и добавка в неполном объеме.
Лейте продукт медленно в небольшом потоке — это мешает ему разрушать баланс pH так же, как если бы вы добавили его резко. При необходимости повторяйте все эти шаги каждые 6 часов, пока бассейновая вода не будет сбалансирована.
Несмотря на то, что бисульфат натрия намного более безопасно использовать и хранить, чем соляную кислоту, важно помнить, что это все еще токсичное вещество, которое должно использоваться с осторожностью.
Не плавайте в бассейне после добавления бисульфата натрия в течение по крайней мере 6 часов. Это может вызвать серьезные ожоги кожи при прямом контакте.
Никогда не добавляйте средства больше, чем рекомендуемое количество. Это может вызвать поверхностное или структурное повреждение для материалов и оборудования.
Источник
Бисульфат натрия — Sodium bisulfate
- 7681-38-1
Y
- 10034-88-5 (моногидрат)
Y
- 56397
Y
- BU8V88OWIQ
Y
- 3KLS9Y77YJ (моногидрат)
Y
138,07 г / моль (моногидрат)
1,8 г / см 3 (моногидрат)
315 ° C (безводный)
100 г / 100 мл (100 ° C)
моноклинная (моногидратная)
 Y проверить ( что есть ?)
Y проверить ( что есть ?)  Y
Y  N
NБисульфат натрия , также известный как гидросульфат натрия , представляет собой натриевую соль бисульфат- аниона с молекулярной формулой NaHSO 4 . Бисульфат натрия представляет собой кислотную соль, образованную частичной нейтрализацией серной кислоты эквивалентом основания натрия, обычно в форме гидроксида натрия (щелочь) или хлорида натрия (поваренная соль). Это сухой гранулированный продукт, который можно безопасно перевозить и хранить. Безводная форма является гигроскопичной . Растворы бисульфата натрия являются кислыми, при этом 1М раствор имеет pH около 1.
СОДЕРЖАНИЕ
Производство
Бисульфат натрия производится в качестве промежуточного продукта в процессе Мангейма , промышленном процессе, включающем реакцию хлорида натрия и серной кислоты :
Этот этап очень экзотермичен. Жидкий бисульфат натрия распыляется и охлаждается, так что он образует твердые шарики. Газообразный хлористый водород растворяют в воде с получением соляной кислоты в качестве полезного побочного продукта реакции.
Хотя это и не представляет коммерческого интереса, бисульфат натрия может быть получен как побочный продукт производства многих других минеральных кислот посредством реакции их натриевых солей с избытком серной кислоты :
Полученные кислоты HX имеют более низкую температуру кипения, чем реагенты, и отделяются от реакционной смеси перегонкой.
Химические реакции
Гидратированный бисульфат натрия дегидратируется при 58 ° C (136 ° F), после чего он отделяется от присоединенной к нему молекулы воды. После повторного охлаждения он становится гигроскопичным. Нагревание бисульфата натрия до 280 ° C (536 ° F) дает пиросульфат натрия , еще одну бесцветную соль:
Использует
Бисульфат натрия используется в первую очередь для снижения pH. он также используется для обработки металлов, чистящих средств и для снижения pH воды для эффективного хлорирования в плавательных бассейнах и гидромассажных ваннах. Бисульфат натрия также одобрен AAFCO в качестве кормовой добавки общего назначения, включая корм для домашних животных. Он используется в качестве подкислителя мочи для уменьшения образования мочевых камней у кошек.
Он очень токсичен для некоторых иглокожих , но довольно безвреден для большинства других форм жизни; поэтому он используется для борьбы со вспышками морских звезд тернового венка .
Бисульфат натрия был основным активным ингредиентом чистящих средств для унитаза Vanish и Sani-Flush , выпуск которых в настоящее время прекращен.
В текстильной промышленности его иногда наносят на бархатную ткань, сделанную с шелковой основой и ворсом волокон на основе целлюлозы (вискоза, хлопок, конопля и т. Д.), Чтобы создать «выгорающий бархат»: бисульфат натрия при нанесении на такие ткани. ткань и нагретая, заставляет волокна на основе целлюлозы становиться хрупкими и отслаиваться, оставляя выжженные участки в готовом материале, обычно в виде привлекательных узоров.
Бисульфат натрия является активным ингредиентом некоторых средств обработки гранулированного помета для домашней птицы, используемых для контроля аммиака. Также было показано, что бисульфат натрия значительно снижает концентрацию Campylobacter и Salmonella в птичниках.
В еде
Бисульфат натрия используется в качестве пищевой добавки к дрожжевым смесям (заставляет их подниматься), а также используется при переработке мяса и птицы, а в последнее время — для предотвращения потемнения свежесрезанных продуктов. Бисульфат натрия считается безопасным (GRAS) FDA. Пищевой продукт также соответствует требованиям Кодекса пищевых химикатов . В ЕС он обозначается E-номером E514ii, а также одобрен для использования в Австралии, Новой Зеландии, Канаде и Мексике. где он указан как добавка 514. Пищевой бисульфат натрия используется в различных пищевых продуктах, включая напитки, приправы, соусы и начинки. Он имеет много синонимов, включая бисульфат соды, кислый сульфат натрия, моногидросульфат натрия, гидросульфат натрия, гидросульфат натрия и натриевую соль серной кислоты (1: 1).
Ассоциация производителей продуктов питания (GMA) считает бисульфат натрия натуральным, поскольку он сделан из минералов. Однако весь имеющийся в продаже бисульфат натрия получают из серной кислоты, синтезированной из элементарной серы посредством контактного процесса .
Бисульфат натрия снижает pH без кислого вкуса и используется вместо коммерчески доступных лимонной, яблочной или фосфорной кислот, а также может использоваться в качестве средства против потемнения.
Источник
HimMax
Каталог
Бисульфат натрия
Бисульфат натрия
ТУ 6-09-3675-74
Гидросульфат натрия (кислый сернокислый натрий, бисульфат натрия) — кислая соль натрия и серной кислоты с формулой NaHSO4, бесцветные кристаллы. Образует кристаллогидрат NaHSO4·H2O. Гидросульфат натрия представляет собой белое сухое кристаллическое вещество плотностью 2,476 кг/куб.дм; безводный продукт сильно гигроскопичен.
Получение гидросульфата натрия (кислый сернокислый натрий, бисульфат натрия)
Распространены 2 промышленных метода. В обоих один из реагентов — серная кислота, а второй — гидроксид или хлорид натрия. Полученный водный раствор целевого продукта затем формируют в гранулы; целесообразно купить гидросульфат натрия именно в гранулированном виде, гораздо более удобном для применения и хранения.
- Гидросульфат натрия получают действием избытка концентрированной серной кислоты на едкий натр:
Физические свойства гидросульфата натрия (кислый сернокислый натрий, бисульфат натрия)
- Гидросульфат натрия образует бесцветные кристаллы триклинной сингонии, пространственная группа P 1 , параметры ячейки a = 0,7005 нм , b = 0,7125 нм , c = 0,6720 нм , α = 95,93° , β = 92,31° , γ = 75,52° , Z = 4 . При нагревании претерпевает два полиморфных перехода при 140 и 170 °C.
- Кристаллогидрат гидросульфата натрия — бесцветные гигроскопические кристаллы моноклинной сингонии, пространственная группа A a, параметры ячейки a = 0,8213 нм , b = 0,7812 нм , c = 0,7805 нм , β = 120,04° , Z = 4 .
Химические свойства гидросульфата натрия (кислый сернокислый натрий, бисульфат натрия)
- При нагревании гидросульфат натрия переходит в пиросульфат натрия:
- При подщелачивании гидросульфат натрия переходит в сульфат:
- При спекании гидросульфат натрия взаимодействует с солями:

| Общие | |
|---|---|
| Систематическое наименование | Гидросульфат натрия |
| Традиционные названия | Кислый сернокислый натрий, бисульфат натрия |
| Хим. формула | NaHSO4 |
| Физические свойства | |
| Состояние | бесцветные кристаллы |
| Молярная масса | 120 г/моль |
| Плотность | 2,472 г/см³ |
| Термические свойства | |
| Т. плав. | 186 °C |
| Химические свойства | |
| Растворимость в воде | 28,6 0 ; 50 100 г/100 мл |
Применение гидросульфата натрия (кислый сернокислый натрий, бисульфат натрия)
- Как флюс в цветной металлургии.
- Как реагент для перевода труднорастворимых окислов в растворимые сульфаты.
- Зарегистрирован в качестве пищевой добавки E514.
- в виде порошка или гранул в качестве реагента, понижающего уровень рН в бассейнах
Легкая и пищевая промышленность, металлообработка, коммунальное хозяйство, прикладные отрасли. Используется прежде всего как подкисляющий реагент с доступной ценой.
В промышленности гидросульфат натрия применяется в составе растворов для отделки кожи и текстильных материалов, а также при финишной обработке металлов: гальванизации, лакировании и др. Значительны объемы его использования в виде компонента бытовых чистящих средств. Также этот реагент применяется для подкисления воды в процессе хлорирования, например, при обеззараживании бассейнов.
Гидросульфат натрия одобрен как пищевая добавка в корма домашних животных; в этом направлении его назначение заключается в снижении щелочности мочи, что способствует предупреждению мочекаменной болезни у кошек. Гидросульфат натрия признан также безопасной пищевой добавкой в продовольственные продукты для человека ( обозначение E514ii по номенклатуре Евросоюза). Обладает уникальной особенностью — снижает pH среды без придания кислого вкуса; в таком качестве гидросульфат натрия используется в производстве множества продуктов питания: напитков, соусов и т.д. Актуально его применение в колбасных изделиях — гидросульфат натрия ингибирует нежелательное изменение цвета готового продукта при контакте с атмосферным кислородом.
В ювелирной отрасли гидросульфат натрия служит основой травильных растворов, удаляющих слой окислов с поверхностей, подвергнутых нагреванию в ходе ювелирной обработки.
Источник