Бассейн передней межжелудочковой артерии
Артерии сердца — аа. coronariae dextra et sinistra, венечные артерии, правая и левая, начинаются от bulbus aortae ниже верхних краев полулунных клапанов. Поэтому во время систолы вход в венечные артерии прикрывается клапанами, а сами артерии сжимаются сокращенной мышцей сердца. Вследствие этого во время систолы кровоснабжение сердца уменьшается: кровь в венечные артерии поступает во время диастолы, когда входные отверстия этих артерий, находящиеся в устье аорты, не закрываются полулунными клапанами.
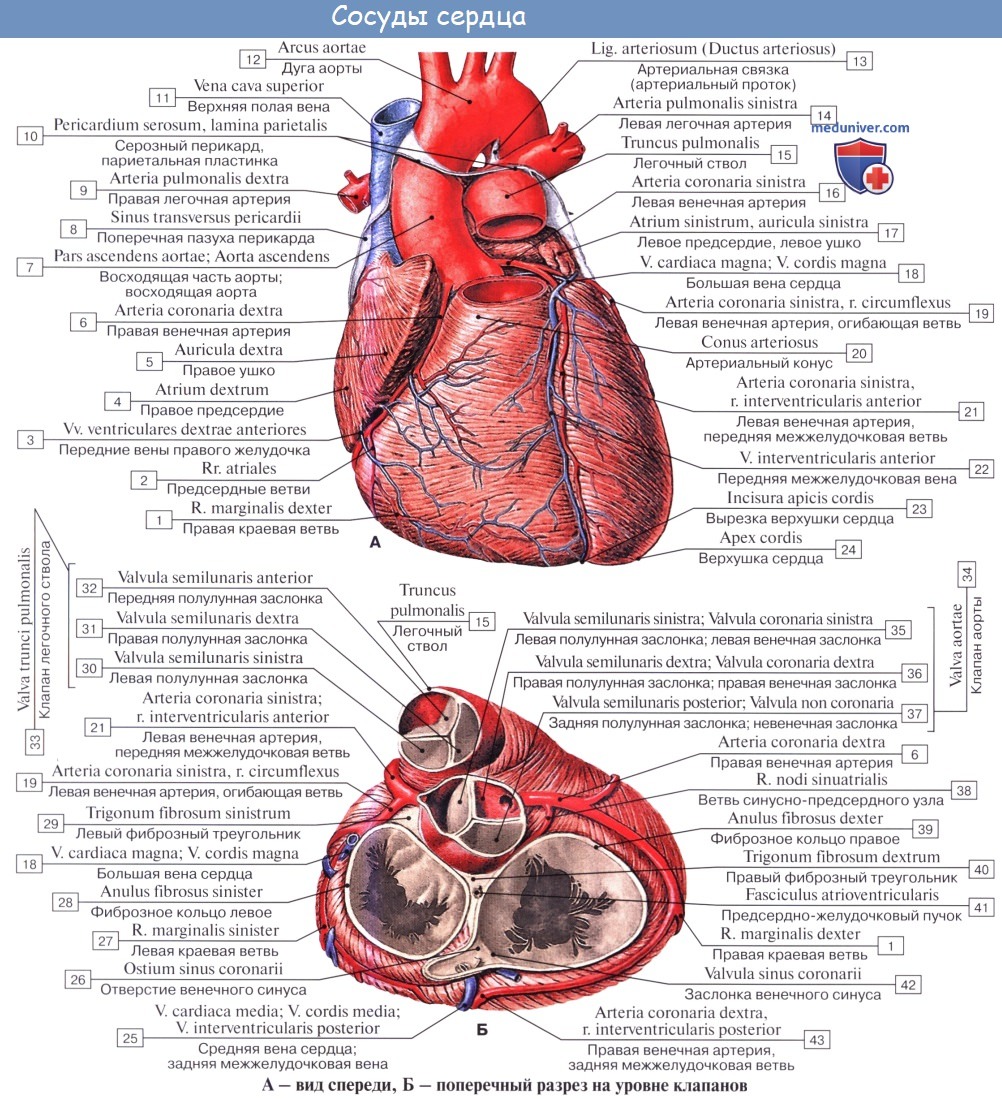
Правая венечная артерия, a. coronaria dextra
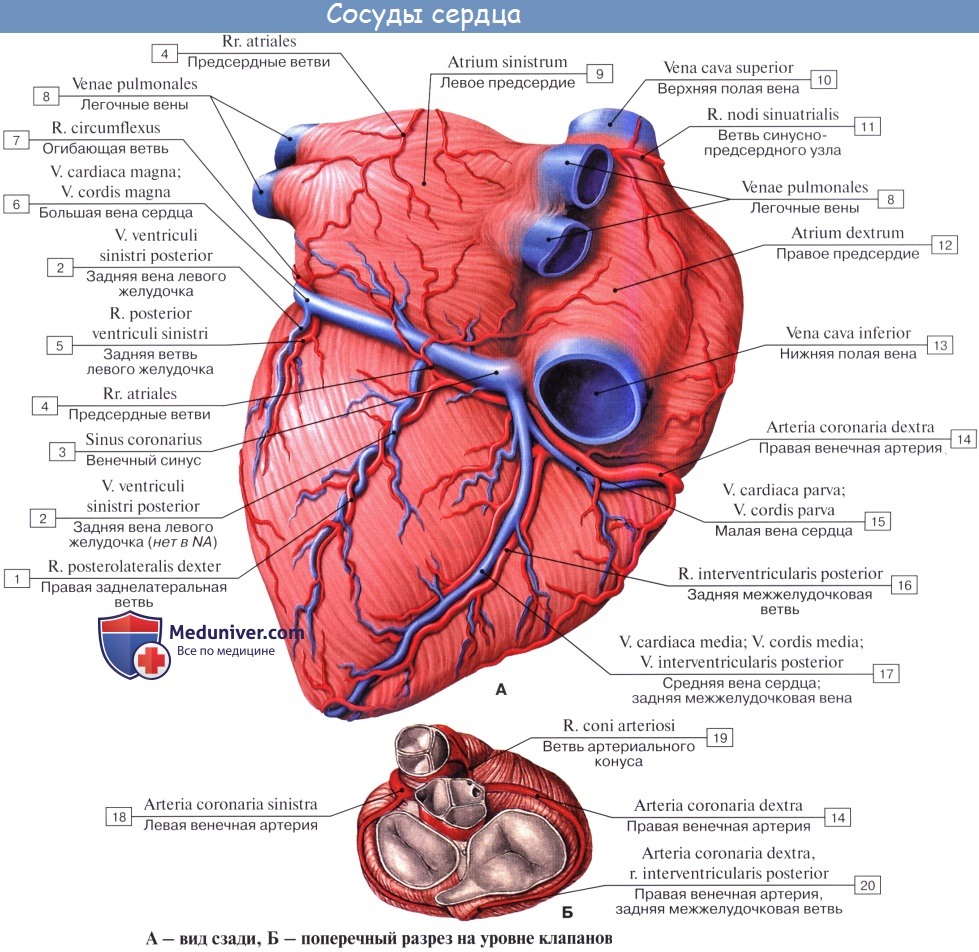
Правая венечная артерия, a. coronaria dextra, выходит из аорты соответственно правой полулунной заслонке и ложится между аортой и ушком правого предсердия, кнаружи от которого она огибает правый край сердца по венечной борозде и переходит на его заднюю поверхность. Здесь она продолжается в межжелудочковую ветвь, r. interventricularis posterior. Последняя спускается по задней межжелудочковой борозде до верхушки сердца, где анастомозирует с ветвью левой венечной артерии.
Ветви правой венечной артерии васкуляризируют: правое предсердие, часть передней стенки и всю заднюю стенку правого желудочка, небольшой участок задней стенки левого желудочка, межпредсердную перегородку, заднюю треть межжелудочковой перегородки, сосочковые мышцы правого желудочка и заднюю сосочковую мышцу левого желудочка. ,
Левая венечная артерия, a. coronaria sinistra
Левая венечная артерия, a. coronaria sinistra, выйдя из аорты у левой полулунной заслонки ее, также ложится в венечную борозду кпереди от левого предсердия. Между легочным стволом и левым ушком она дает две ветви: более тонкую переднюю, межжелудочковую, ramus interventricularis anterior, и более крупную левую, огибающую, ramus circumflexus.
Первая спускается по передней межжелудочковой борозде до верхушки сердца, где она анастомозирует с ветвью правой венечной артерии. Вторая, продолжая основной ствол левой венечной артерии, огибает по венечной борозде сердце с левой стороны и также соединяется с правой венечной артерией. В результате по всей венечной борозде образуется артериальное кольцо, расположенное в горизонтальной плоскости, от которого перпендикулярно отходят ветви к сердцу.
Кольцо является функциональным приспособлением для коллатерального кровообращения сердца. Ветви левой венечной артерии васкуляризируют левое, предсердие, всю переднюю стенку и большую часть задней стенки левого желудочка, часть передней стенки правого желудочка, передние 2/3 межжелудочковой перегородки и переднюю сосочко-вую мышцу левого желудочка.
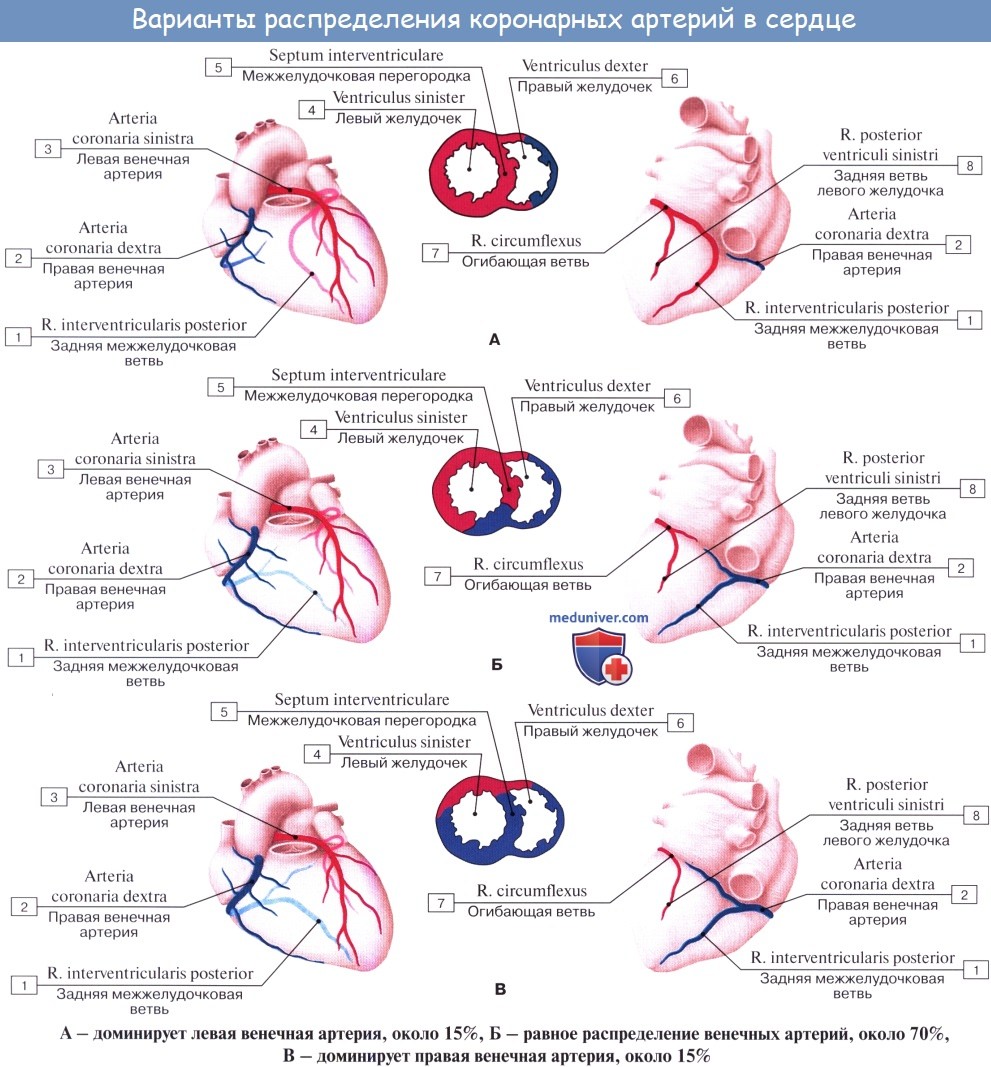
Наблюдаются различные варианты развития венечных артерий, вследствие чего имеются различные соотношения бассейнов кровоснабжения. С этой точки зрения различают три формы кровоснабжения сердца: равномерную с одинаковым развитием обеих венечных артерий, левовенечную и правовенеч-ную. Кроме венечных артерий, к сердцу подходят «дополнительные» артерии от бронхиальных артерий, от нижней поверхности дуги аорты вблизи артериальной связки, что важно учитывать, чтобы не повредить их при операциях на легких и пищеводе и этим не ухудшить кровоснабжение сердца.
Внутриорганные артерии сердца
Внутриорганные артерии сердца: от стволов венечных артерий и их крупных ветвей соответственно 4 камерам сердца отходят ветви предсердий (rr. atriales) и их ушек (rr. auriculares), ветви желудочков (rr. ventriculares), перегородочные ветви (rr. septales anteriores et posteriores). Проникнув в толщу миокарда, они разветвляются соответственно числу, расположению и устройству слоев его: сначала в наружном слое, затем в среднем (в желудочках) и, наконец, во внутреннем, после чего проникают в сосочковые мышцы (аа. papillares) и даже в предсердно-желудоч-ковые клапаны. Внутримышечные артерии в каждом слое следуют ‘ходу мышечных пучков и анастомозируют во всех слоях и отделах сердца.
Некоторые из этих артерий имеют в своей стенке сильно развитый слой непроизвольных мышц, при сокращении которых происходит полное замыкание просвета сосуда, отчего эти артерии называют «замыкающими». Временный спазм «замыкающих» артерий может повлечь за собой прекращение тока крови к данному участку сердечной мышцы и вызвать инфаркт миокарда.
Источник
Интрамуральный ход коронарных артерий: обзор литературы и клиническое наблюдение
В статье представлен обзор литературы, касающейся интрамурального хода коронарных артерий с формированием миокардиальных «мостиков». Уделено внимание аспектам распространенности, клинических проявлений, современных методов диагностики, а также вопросам вы
The article reviews intramyocardial course of coronary arteries with myocardial bridging. This report describes the prevalence, clinical presentation, evaluation, and management of adults with symptomatic myocardial bridges.
Общепризнано, что развитие острого коронарного синдрома (ОКС) является прерогативой лиц старшей возрастной группы. Однако аналогичная симптоматика может наблюдаться и у лиц молодого возраста, еще не подверженных атеросклерозу и атеротромбозу. Особая клиническая значимость изучения ОКС у молодых связана с тем, что в ряде случаев ОКС завершается развитием острого инфаркта миокарда или внезапной сердечной смерти.
Наиболее частой причиной развития ОКС у лиц молодого возраста являются врожденные аномалии развития коронарных артерий (КА), представленные изменением числа сосудов, расположением основных стволов и их устьев [1–5]. Самой распространенной аномалией хода КА считается их прохождение в толще миокарда — интрамуральный, или «ныряющий», ход [6].
Мышца, покрывающая интрамуральный («туннельный») сегмент КА, называется миокардиальным «мостиком» (ММ). Частота встречаемости ММ по данным разных авторов существенно различается и зависит как от характеристик выборки, так и от использованного метода диагностики. Так, сообщается, что при коронароангиографии распространенность ММ колеблется в пределах
Г. И. Нечаева, доктор медицинских наук, профессор
И. В. Друк, доктор медицинских наук, профессор
Ю. В. Терещенко 1 , кандидат медицинских наук
М. И. Шупина, кандидат медицинских наук
Е. Н. Логинова, кандидат медицинских наук
Е. В. Надей
ФГБОУ ВО ОмГМУ МЗ РФ, Омск
Интрамуральный ход коронарных артерий: обзор литературы и клиническое наблюдение/ Г. И. Нечаева, И. В. Друк, Ю. В. Терещенко, М. И. Шупина, Е. Н. Логинова, Е. В. Надей
Для цитирования: Лечащий врач № 2/2018; Номера страниц в выпуске: 10-13
Теги: сердце, дисплазия соединительной ткани
Источник
Миокардиальные мышечные «мостики»
… являются одной из причин нарушения коронарного кровообращения с развитием ишемии миокарда вплоть до некроза.

В зарубежной литературе встречаются различные определения: «мышечная перемычка», «мышечный мост» или «интрамуральная левая передняя нисходящая артерия». Наиболее часто встречается определение «миокардиальный мостик (ММ) левой передней нисходящей артерии (ЛПНА)» (ММ чаще всего встречаются над ЛПНА в проксимальной или средней трети, и в передней межжелудочковой ветви (ПМЖВ) чаще у молодых мужчин; изредка ММ встречается в области огибающей артерии; значительно реже ММ локализуется над другими эпикардиальными артериями, что чаще всего при гипертрофической кардиомиопатии).
ММ появляются в эмбриональный период развития параллельно с формированием коронарных артерий и представляют собой вариант нормы или врожденную анатомическую аномалию развития и формирования сосудистой системы сердца и миокарда. По данным морфологических исследований, длина ММ колеблется от 4 до 40 мм (наиболее часто от 10 до 19 мм), толщина в среднем составляет 2,8 мм.
ММ — частая находка, их обнаруживают в 30%случаев всех аутопсий, при этом при ангиографии они обнаруживаются в 5% случаев, возможно из-за того, что тонкие ММ вызывают незначительную компрессию коронарных артерий во время систолыи не видны при коронарографии (после использования провокационных тестов — внутрикоронарное введение ацетилхолина или эргометрина, способствующих систолическому сжатию туннелированной артерии, увеличивающих силу и частоту сердечных сокращений, — частота обнаружения ММ при ангиографии может возрастать до 40%).
Поскольку ММ – это частая находка при аутопсии в норме, некоторые авторы считают её доброкачественным анатомическим изменением. Данная мальформация присутствует с рождения, но ей клинические симптомы обычно не развиваются до третьей декады жизни.
Наличие систолического сужения просвета артерии в месте ММ может вызвать нарушение коронарного кровотока, несмотря на то, что для кровоснабжения миокарда определяющее значение имеет кровоток в диастолу. Установлена связь наличия ММ с приступами стенокардии, инфарктом миокарда и внезапной смертью после значительной физической нагрузки, особенно при наличии гипертрофии миокарда левого желудочка и тахикардии. Ишемия миокарда, инфаркт, внезапная сердечная смерть у детей, подростков и молодых людей очень редко вызываются атеросклерозом, зачастую причиной такой патологии в детском и юном возрасте становятся аномалии коронарных артерий, в том числе и их интрамуральное расположение. Факторами, способствующими развитию ишемии миокарда, являются коронарный спазм, тахикардия, возникающая при физических нагрузках и уменьшающая продолжительность диастолического наполнения коронарных артерий, тромбоз в месте ММ.
Клинически наличие глубоко расположенных ММ может проявляться болями стенокардического характера, инфарктом миокарда, желудочковыми нарушениями ритма, преходящей атриовентрикулярной блокадой, внезапной остановкой сердца. Эти осложнения очень редки и, вероятно, связаны с выраженной компрессией коронарных сосудов при глубоком залегании в толще миокарда. Нагрузочные тесты могут индуцировать появление на ЭКГ неспецифических признаков ишемии миокарда, нарушение внутри-желудочковой проводимости или аритмии, которые на ЭКГ покоя не регистрировали. Диагноз клинически выраженного ММ должен быть поставлен у пациентов, которые имеют стенокардию без традиционных факторов риска и признаков ишемии.
Современный «золотой стандарт» для диагностики ММ — это коронарная ангиография. Типичными ангиографическими проявлениями ММ считают «milking effeсt» и «step down-step up» феномены, обусловленные систолической компрессией туннелированного сегмента коронарной артерии. Феномен «milking» («молочный эффект», эффект выдаивания или выдавливания) характеризуется сужением коронарной артерии в фазу систолы и полным или частичным расправлением в фазу диастолы (эффект выдавливания контрастного вещества при сужении интрамуральной части коронарной артерии во время систолы — систолическая компрессия туннелированного сегмента). Многие авторы считают «эффект выдавливания» основным диагностическим ангиографическим признаком ММ. Феномен «step down-step up» заключается в фазовом «пошаговом» заполнении контрастом туннелированной артерии. Многие авторы считают «эффект выдавливания» основным диагностическим ангиографическим признаком ММ.
Значимость систолического и диастолического сужения может подтвердить внутрисосудистое ультразвуковое исследование (ВСУЗИ), которое может измерить не только диаметр, но и площадь просвета при несферическом просвете сосуда. Мультиспиральная компьютерная томография (МСКТ) также является эффективным неинвазивным методом диагностики ММ, с помощью которого можно определить длину и глубину расположения туннелированной артерии, ее диаметр и процент стеноза на уровне ММ во время систолы и диастолы. Кроме того, МСКТ эффективна для визуализации других аномалий коронарных артерий, миокарда, эпикарда и близлежащих образований грудной клетки.
Обратите внимание! При определенных условиях наличие ММ может служить причиной внезапной смерти, поэтому все пациенты с миокардиальными «мостиками» и клиническими их проявлениями должны находиться под врачебным контролем. Медикаментозная терапия должна быть методом выбора лечения клинически значимых ММ, а хирургическое вмешательство должно ограничиваться пациентами со стенокардией, рефрактерной к медикаментозной терапии. Принципы лечения этих пациентов в основном не отличаются от методов лечения пациентов с ИБС и поражением одного сосуда.
Медикаментозная терапия должна включать бета-блокаторы, блокаторы кальциевых каналов и антитромбоцитарные агенты. Цель терапии – освобождение от симптомов и признаков ишемии миокарда, профилактика будущих коронарных событий. Обычно в качестве препаратов первой линии применяют бета-блокаторы. ! Важно помнить, что нитраты могут ухудшать состояние таких пациентов, а нагрузка жидкостью, напротив, – увеличивать сопротивление сосудов к компрессии и уменьшать ишемию. Следовательно, классические антиангинальные подходы в случае ишемии, обусловленной интрамуральным прохождением коронарной артерии, не только неэффективны,но и могут усугубить нарушения перфузии миокарда.
У больных, рефрактерных к фармакотерапии, используется хирургическое рассечение мышечных мостиков, аортокоронарное шунтирование и стентирование данного сегмента коронарной артерии. Показания к стентированию или хирургическому лечению при наличии клинически значимого ММ можно выставить, когда доказаны клинические проявления ишемии миокарда. Для этого применяются нагрузочные тесты, стресс-эхокардиография, суточное мониторирование ЭКГ и радиоизотопные методы с физической нагрузкой. Необходимо отметить, что стентирование коронарных артерий часто (в 50% случаев) связано с рестенозами и перипроцедурными осложнениями (Mohlenkamp S, Hort W, Ge J, Erbel R.; 2002).
Рекомендации для спортсменов:
- 1. Спортсмены с ММ при условии отсутствия ишемии миокарда в покое и при физической нагрузке могут быть допущены к занятиям всеми видами спорта.
2. Спортсмены с ММ и объективными признаками скрытой ишемии миокарда или перенесенным инфарктом миокарда в анамнезе могут быть допущены к занятиям низкоинтенсивными видами спорта (класс IA).
3. Спортсмены, перенесшие операцию по рассечению мышечных мостиков или стентирование, могут быть допущены к занятиям низкоинтенсивными видами спорта на срок не менее 6 мес после вмешательства. Асимптомным спортсменам для решения вопроса о допуске к занятиям спортом необходимо проведение нагрузочного теста. В случае нормальной толерантности к физической нагрузке и отсутствии признаков скрытой ишемии миокарда спортсмены могут быть допущены к занятиям всеми видами спорта.
Источник